
分析 (1)①漂白粉的主要成分是次氯酸钙[Ca(ClO)2]和氯化钙,氯气与石灰乳反应产物是氯化钙、次氯酸钙和水;
②次氯酸的酸性弱于碳酸,根据强酸制弱酸原理,漂白粉溶于水后,受空气中的CO2作用,生成CaCO3和HClO;
(2)通过CO、NO的化合价分析,可以猜测出“无毒气体”的成分是N2和CO2.
解答 解:(1)①漂白粉的主要成分是次氯酸钙[Ca(ClO)2]和氯化钙,工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,同时有水生成,反应的化学方程式为:2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O,
故答案为:2Cl2+2 Ca(OH)2═Ca(ClO)2+CaCl2+2H2O;
②HClO虽是强氧化性的酸,但它是比碳酸还弱的酸,漂白粉溶于水后,受空气中的CO2作用,生成CaCO3和HClO,该反应的化学方程式为:Ca(ClO)2+H2O+CO2═CaCO3 ↓+2HClO,
故答案为:Ca(ClO)2+H2O+CO2═CaCO3 ↓+2HClO;
(2)在汽车尾气排放管中安装一个催化转化器,可将尾气中另一种有害气体CO跟NO反应转化为无毒气体二氧化碳和氮气,从CO、NO的化合价分析,可以猜测出“无毒气体”的成分是N2和CO2,原理方程式为:2NO+2CO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2,
故答案为:2NO+2CO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2.
点评 本题考查学生书写化学方程式的能力,把握发生的化学反应为解答的关键,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等,题目难度不大.


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A | B | C | |
| D | E |
| A. | A与B形成的阴离子可能有AB32-、A2B42- | |
| B. | AD2分子中每个原子的最外层均为8电子结构 | |
| C. | C和E氢化物的热稳定性和还原性均依次减弱 | |
| D. | A、D、E的最高价氧化物对应的水化物的酸性依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
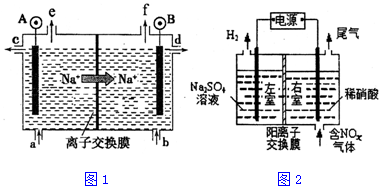
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
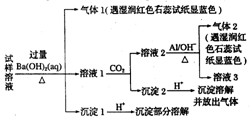 最近一段时间,武邑中学雾霾严重,影响了同学们的生活和健康.雾霾中可能含有如下离子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-.高三1490班某同学收集了操场的雾霾,经必要的预处理后得试样溶液,设计并完成了如下实验,根据实验操作与现象,该同学得出的结论不正确的是( )【已知:3NO3-+8Al+5OH-+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$3NH3↑+8AlO2-】
最近一段时间,武邑中学雾霾严重,影响了同学们的生活和健康.雾霾中可能含有如下离子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-.高三1490班某同学收集了操场的雾霾,经必要的预处理后得试样溶液,设计并完成了如下实验,根据实验操作与现象,该同学得出的结论不正确的是( )【已知:3NO3-+8Al+5OH-+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$3NH3↑+8AlO2-】| A. | 试样中一定存在的阴离子是SO42-和NO3- | |
| B. | 试样中一定不含Al3+ | |
| C. | 该雾霾中可能存在NaNO3、NH4Cl和MgSO4 | |
| D. | 试样中可能存在Na+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 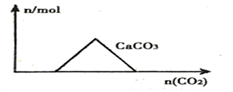 向Ca(OH)2和NaOH的混合溶液中通入CO2 | |
| B. | 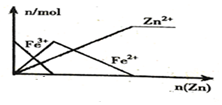 向FeCl3溶液中加入锌粉 | |
| C. | 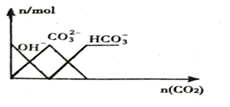 向NaOH溶液中通入CO2 | |
| D. | 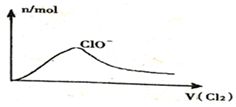 Cl2通入NaOH溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a<b | B. | a>b | C. | a=b | D. | 2b=a |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 起始浓度(mol/L) | 甲 | 乙 | 丙 |
| C(H2) | 0.010 | 0.020 | 0.020 |
| C(CO2) | 0.010 | 0.010 | 0.020 |
| A. | 反应开始时,丙中的反应速率最快,甲中的反应速率最慢 | |
| B. | 平衡时,甲、乙、丙中CO2的转化率有如下关系:乙>甲=丙=60% | |
| C. | 平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L | |
| D. | 改变条件使乙中温度降低,新平衡中H2的浓度增大,则正反应的△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 古文或谚语 | 化学解释 |
| A | 蜡炬成灰泪始干 | “泪”就是蜡烛燃烧产生的水 |
| B | 以曾青涂铁,铁赤色如铜 | 置换反应 |
| C | 真金不怕火炼 | 金的活动性顺序排最后,性质稳定 |
| D | 野火烧不尽,春风吹又生 | 涉及氧化还原反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com