
【题目】下列说法正确的是
A. 有机反应中常说的卤化、硝化、水化都属于取代反应
B. 按系统命名法,有机物 的名称为:2,2,4—三甲基—4—戊烯
的名称为:2,2,4—三甲基—4—戊烯
C. 分子式为C8H11N的有机物,分子内含有苯环和氨基(-NH2)的同分异构体共13种
D. 废旧钢材焊接前,分别用饱和Na2CO3、NH4Cl溶液处理焊点
科目:高中化学 来源: 题型:
【题目】![]() 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
A.0.1 mol 的![]() 中,含有
中,含有![]() 个中子
个中子
B.pH=1的H3PO4溶液中,含有![]() 个
个![]()
C.2.24L(标准状况)苯在O2中完全燃烧,得到![]() 个CO2分子
个CO2分子
D.密闭容器中1 mol PCl3与1 mol Cl2反应制备 PCl5(g),增加![]() 个P-Cl键
个P-Cl键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,干燥圆底烧瓶中充满NO2和O2的混合气体进行喷泉实验,经充分反应后,瓶内充满水,则瓶内水溶液的物质的量浓度为
A. 5/112 B. 1/28 C. 2/49 D. 8/245
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了将混有K2SO4、MgSO4的KNO3固体提纯,并制得纯净的KNO3溶液,某学生设计如下实验方案:
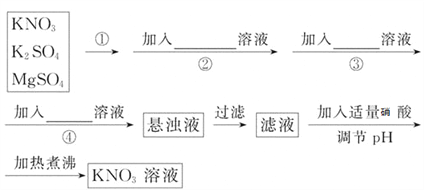
(1)操作①为___________________________。
(2)操作②~④加入的试剂依次可以为:____________________________。
(3)如何判断SO42-已除尽?____________________________。
(4)加热煮沸的目的:___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(17分)
羟甲香豆素是一种治疗胆结石的药物,合成路线如下图所示:

已知: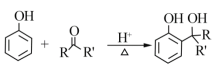
RCOOR'+R'OH![]() RCOOR'+ R'OH(R、R'、R'代表烃基)
RCOOR'+ R'OH(R、R'、R'代表烃基)
(1)A属于芳香烃,其结构简式是______________________。B中所含的官能团是________________。
(2)C→D的反应类型是___________________。
(3)E属于脂类。仅以乙醇为有机原料,选用必要的无机试剂合成E,写出有关化学方程式:______________________________。
(4)已知:2E![]() F+C2H5OH。F所含官能团有
F+C2H5OH。F所含官能团有![]() 和___________。
和___________。
(5)以D和F为原料合成羟甲香豆素分为三步反应,写出有关化合物的结构简式:

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列性质中,能充分说明某晶体一定是离子晶体的是
A.具有较高的熔点,硬度大B.固态不导电,水溶液能导电
C.晶体中存在金属阳离子,熔点较高D.固态不导电,熔融状态能导电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种化工原料,在工业生产中有重要的应用。
Ⅰ.在l.0L恒容密闭容器中投入1 molCO2和2.75molH2发生反应:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图所示,下列说法正确的是_______。
CH3OH(g)+H2O(g),实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图所示,下列说法正确的是_______。


A.该反应的正反应为放热反应
B.压强大小关系为pl<p2<p3
c. M点对应的平衡常数K的值约为1.04×10-2
D.在p2及512K时,图中N点v(正)<v(逆)
Ⅱ.甲醇是基本有机化工原料。甲醇及其可制得的产品的沸点如下。
名称 | 甲醇 | 二甲胺 | 二甲基甲酰胺 | 甲醚 | 碳酸二甲酯 |
结构简式 | CH3OH | (CH3)2NH | (CH3)2NCHO | CH3OCH3 | (CH3O)2CO |
沸点/℃ | 64.7 | 7.4 | 153 | -24.9 | 90 |
(1)在425℃、Al2O3做催化剂,甲醇与氨气反应可以制得二甲胺。二甲胺显弱碱性,与盐酸反应生成(CH3)2NH2Cl,溶液中各离子浓度由大到小的顺序为____________。
(2)甲醇制甲醚的化学方程式为2CH3OH![]() CH3OCH3+H2O,一定温度下,在体积为1.0L的恒容密闭容器中发生该反应。己知387℃时该反应的化学平衡常数K=4,若起始时向容器I中充入0.10molCH3OH、0.15molCH3OCH3和0.10molH2O,则反应将向______(填“正”或“逆”)反应方向进行。
CH3OCH3+H2O,一定温度下,在体积为1.0L的恒容密闭容器中发生该反应。己知387℃时该反应的化学平衡常数K=4,若起始时向容器I中充入0.10molCH3OH、0.15molCH3OCH3和0.10molH2O,则反应将向______(填“正”或“逆”)反应方向进行。
(3)以甲醇为主要原料,电化学合成碳酸二甲酯的工作原理如下图所示。
电源的负极为__________(填“A”或“B”),写出阳极的电极反应_________;若参加反应的O2为1.12m3(标准状况),则制得的碳酸二甲酯的质量为______kg。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】非金属元素H、C、O、S、Cl能形成的化合物种类很多,单质及化合物的用途很广泛。
(1)O2的电子式为 。
(2)O、Cl两元素形成的单质和化合物常用来杀菌消毒,试举例________(化学式,任写两种)。
(3)CH3OH在常温下为液态,沸点高于乙烷的主要原因是 。
(4)Cl2是一种大气污染物,液氯储存区贴有的说明卡如下(部分):
危险性 |
|
储运要求 | 远离金属粉末、氨、烃类、醇类物质;设置氯气检测仪 |
泄漏处理 | NaOH、NaHSO3溶液吸收 |
包装 | 钢瓶 |
①用离子方程式表示“泄漏处理”中NaHSO3溶液的作用: 。
②若液氯泄漏后遇到苯,在钢瓶表面氯与苯的反应明显加快,原因是 。
③将Cl2通入适量KOH溶液中,产物中可能有KCl、KClO、KClO3。当溶液中c(Cl)∶c(ClO)=11∶1时,则c(ClO)∶c(![]() )比值等于 。
)比值等于 。
(5)镁是一种较活泼的金属, Mg与Ca类似,也能与C形成某种易水解的离子化合物。已知该化合物0.1 mol与水完全反应后,产生0.1 mol的某种气体。该气体被溴水全部吸收后,溴水增重2.6 g。请写出该水解反应方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 [实验化学]
1-溴丙烷是一种重要的有机合成中间体,沸点为71℃,密度为1.36 g·cm-3。实验室制备少量1-溴丙烷的主要步骤如下:
步骤1: 在仪器A中加入搅拌磁子、12 g正丙醇及20 mL水,冰水冷却下缓慢加入28 mL浓H2 SO4 ;冷却至室温,搅拌下加入24 g NaBr。
步骤2: 如图所示搭建实验装置, 缓慢加热,直到无油状物馏出为止。
步骤3: 将馏出液转入分液漏斗,分出有机相。
步骤4: 将分出的有机相转入分液漏斗,依次用12 mL H2O、12 mL 5% Na2CO3溶液和12 mL H2O洗涤,分液,得粗产品,进一步提纯得1-溴丙烷。

(1)仪器A的名称是_____________;加入搅拌磁子的目的是搅拌和___________________。
(2)反应时生成的主要有机副产物有2-溴丙烷和__________________________________。
(3)步骤2中需向接受瓶内加入少量冰水并置于冰水浴中的目的是___________________。
(4)步骤2中需缓慢加热使反应和蒸馏平稳进行,目的是______________________________。
(4)步骤4中用5%Na2CO3溶液洗涤有机相的操作: 向分液漏斗中小心加入12 mL 5% Na2CO3溶液,振荡,____________,静置,分液。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com