
| A. | 甲烷、乙烯和苯都可以从化石燃料中提取,都能使溴水因发生化学反应而褪色 | |
| B. | 乙烯和苯分子中因都存在C═C,因为都能发生加成反应和氧化反应 | |
| C. | 酸性KMnO4溶液既可鉴别乙烷与乙烯,又可除去乙烷中的乙烯而得到纯净的乙烷 | |
| D. | 只用一种试剂就可以鉴别乙醇、乙酸、四氯化碳、苯四种液体 |
分析 A、甲烷与苯均不和溴水反应;
B、苯分子不存在C=C双键,存在的是一种特殊的化学键;
C、乙烯被高锰酸钾溶液氧化为二氧化碳气体,也是乙烷中的杂质气体;
D、苯、四氯化碳都不溶于水,乙酸与碳酸钠反应放出二氧化碳气体,乙醇和水混溶,结合密度大小可鉴别.
解答 解:A、甲烷、苯不能和溴水反应使其褪色,故A错误;
B、苯分子中的化学键是介于单键与双键之间的特殊化学键,不是双键,故B错误;
C、酸性高锰酸钾可以鉴别乙烷与乙烯,由于与乙烯反应生成新的杂质气体二氧化碳,故不能应用于乙烷的除杂,故C错误;
D、苯、四氯化碳都不溶于水,且苯在上层,四氯化碳在下层,乙酸与碳酸钠反应放出二氧化碳气体,乙醇和水混溶,故可以利用碳酸钠溶液进行鉴别四种液体,故D正确,故选D.
点评 本题主要考查的是常见有机化合物的性质、苯的结构、气体除杂与鉴别等,综合性较强,难度不大.


 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | X的氢氧化物是一种强碱 | B. | X的碳酸正盐不溶于水 | ||
| C. | X原子核外有6个电子层 | D. | X的最高化合价为+2价 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2 (g) (红棕色)═N2O4(g) (无色),如图所示.
在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2 (g) (红棕色)═N2O4(g) (无色),如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 等质量的金刚石与石墨完全燃烧,放出的能量一样多 | |
| B. | 等质量的金刚石与石墨完全燃烧,石墨放出的能量少 | |
| C. | 石墨不如金刚石稳定 | |
| D. | 金刚石不如石墨稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 反应时间/min | n(A)/mol | n(B)/mol |
| 0 | 4 | 4 |
| 0.5 | 3.2 | |
| 2 | 2.4 | |
| 3 | 1.0 |
| A. | 反应在前0.5min时,n(W)=0.6mol | |
| B. | 2min时,反应的平均反应速率为V(Q)=0.48mol/L•s | |
| C. | 相同温度条件下,向平衡后的容器中再充入2mol Q和2mol W时,v(正)>v(逆) | |
| D. | 相同温度下,平衡时的平衡常数为27L•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 流动电池是一种新型电池.其主要特点是可以通过电解质溶液的循环流动,在电池外部调节电解质溶液,以保持电池内部电极周围溶液浓度的稳定.北京化工大学新开发的一种流动电池如图所示,电池总反应为Cu+PbO2+2H2SO4═CuSO4+PbSO4+2H2O.下列说法不正确的是( )
流动电池是一种新型电池.其主要特点是可以通过电解质溶液的循环流动,在电池外部调节电解质溶液,以保持电池内部电极周围溶液浓度的稳定.北京化工大学新开发的一种流动电池如图所示,电池总反应为Cu+PbO2+2H2SO4═CuSO4+PbSO4+2H2O.下列说法不正确的是( )| A. | a为负极,b为正极 | |
| B. | 该电池工作时PbO2电极附近溶液的pH增大 | |
| C. | a极的电极反应为Cu-2e-═Cu2+ | |
| D. | 调节电解质溶液的方法是补充CuSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
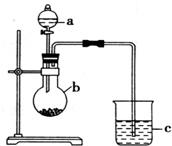 “元素的最高价氧化物对应的水化物酸性越强非金属性越强”某同学欲运用这一观点来验证硫和碳两元素的得电子的能力强弱,设计实验如图所示,请回答:
“元素的最高价氧化物对应的水化物酸性越强非金属性越强”某同学欲运用这一观点来验证硫和碳两元素的得电子的能力强弱,设计实验如图所示,请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com