
| A. | 不慎将苯酚固体粉末沾在皮肤上,立即用大量热水(>65℃)冲洗 | |
| B. | 银氨溶液、Cu(OH)2悬浊液、氯水在实验室里均不宜长期放置 | |
| C. | 检验C2H5Cl中的氯元素:将C2H5Cl与NaOH溶液混合加热,冷却后加AgNO3溶液 | |
| D. | 同温下用pH试纸测定等浓度的NaClO溶液和CH3COONa溶液的pH,可以证明HClO和CH3COOH的酸性强弱 |
分析 A.苯酚具有腐蚀性,在温度大于65℃易溶于水,但温度高的热水对皮肤产生伤害;
B.在实验室中,见光易分解,易被氧化、易与空气中的物质反应的化学试剂不宜长期放置,应在使用时配制;
C.在加入硝酸银溶液之前必须加入稀硝酸中和未反应的NaOH;
D.次氯酸钠溶液能漂白pH试纸.
解答 解:A.苯酚具有腐蚀性,在温度大于65℃易溶于水,但温度高的热水对皮肤产生伤害,应该用酒精,故A错误;
B.在实验室中,见光易分解,易被氧化、易与空气中的物质反应的化学试剂不宜长期放置,应在使用时配制,银氨溶液因转化成易爆的雷酸银而不能长期存放,必须现用现配;氢氧化铜悬浊液易产生沉淀,次氯酸见光易分解,所以这几种物质在实验室不宜长时间放置,故B正确;
C.在加入硝酸银溶液之前必须加入稀硝酸中和未反应的NaOH,否则硝酸银和NaOH反应,故C错误;
D.次氯酸钠溶液能漂白pH试纸,应该用pH计测量溶液的pH值,故D错误;
故选B.
点评 本题考查化学实验方案评价,为高频考点,涉及实验安全、元素测定、pH测定等知识点,明确实验原理及物质性质是解本题关键,注意次氯酸钠、次氯酸的漂白性,易错选项是D.


科目:高中化学 来源: 题型:选择题
| A. | 若原料完全反应生成上述产物,CH2CH2Br与NH3的物质之比为2:1 | |
| B. | 该反应属于取代反应 | |
| C. | CH2CH2Br与HBr均属于电解质 | |
| D. | CH2CH2Br难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C、D、E、F、G、H八种主族元素分布在三个不同的短周期,它们在周期表中位置如下:
A、B、C、D、E、F、G、H八种主族元素分布在三个不同的短周期,它们在周期表中位置如下:
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
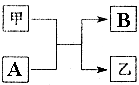 单质A、B与化合物甲、乙有如图所示的转化关系(必要的反应条件未标出),回答下列问题:
单质A、B与化合物甲、乙有如图所示的转化关系(必要的反应条件未标出),回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
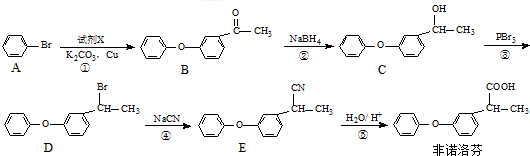
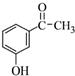 .
.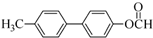 .
. .
.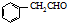 为原料制备
为原料制备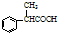 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C=CH2$→_{催化剂}^{H_{2}O}$CH3CH2OH$→_{浓硫酸△}^{CH_{3}COOH}$CH3COOC2H5.
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C=CH2$→_{催化剂}^{H_{2}O}$CH3CH2OH$→_{浓硫酸△}^{CH_{3}COOH}$CH3COOC2H5.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
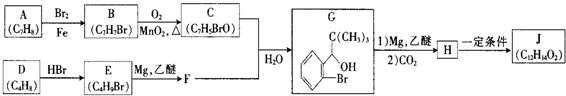
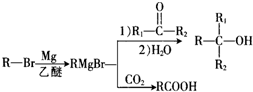
 .
. +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$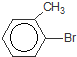 +HBr,反应类型为取代反应.
+HBr,反应类型为取代反应.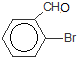 +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$ +Cu2O↓+2H2O.
+Cu2O↓+2H2O. .
. 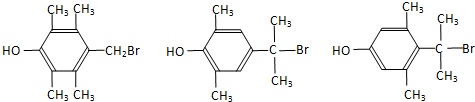 任意2种.
任意2种.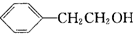
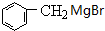 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
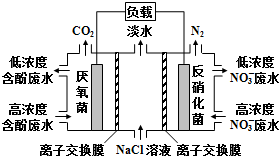
| A. | 右室电极为该电池的正极 | |
| B. | 左室电极反应式可表示为:C6H5OH-28e-+11H2O═6CO2↑+28H+ | |
| C. | 右室电极附近溶液的pH减小 | |
| D. | 工作时中间室的Cl-移向左室,Na+移向右室 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
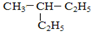 和
和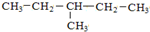
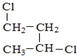 与
与 ④H2O和D2O
④H2O和D2O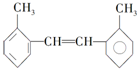 其苯环上的一氯代物有4种;1mol该物质和溴水混合,消耗Br2的物质的量为1mol.
其苯环上的一氯代物有4种;1mol该物质和溴水混合,消耗Br2的物质的量为1mol.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com