
“纳米材料”是粒子直径为1~100nm的材料,纳米碳就是其中一种,若将纳米碳均匀地分散到蒸馏水中,所形成的物质( )
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸 ⑥静置后会析出黑色沉淀
A.①④⑤ B.②③④ C.②③⑤ D.①③④⑥
 习题精选系列答案
习题精选系列答案科目:高中化学 来源:2016届吉林省高三上第三次模拟化学试卷(解析版) 题型:选择题
下列是某兴趣小组根据课本实验设计的一个能说明碳酸钠与碳酸氢钠热稳定性的套管实验,请观察如下图装置、分析实验原理,并判断下列说法和做法,其中不科学的( )
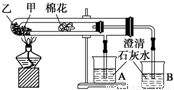
A.甲为小苏打,乙为纯碱
B.要证明碳酸氢钠受热能产生水,可在小试管内塞上沾有无水硫酸铜粉末的棉花球
C.加热不久就能看到A烧杯的澄清石灰水变浑浊
D.整个实验过程中都没有发现A烧杯的澄清石灰水变浑浊
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西柳州铁路第一中学高二上段考理化学卷(解析版) 题型:填空题
根据题目提供的溶度积数据进行计算并回答下列问题:
(1)已知25 ℃时,Ksp[Mg(OH)2]=5.6×10-12;酸碱指示剂百里酚蓝变色的pH范围如下:
pH | <8.0 | 8.0~9.6 | >9.6 |
颜色 | 黄色 | 绿色 | 蓝色 |
25 ℃时,在Mg(OH)2饱和溶液中滴加2滴百里酚蓝指示剂,溶液的颜色为____________。
(2)向50 mL 0.018 mol·L-1的AgNO3溶液中加入50 mL 0.020 mol·L-1的盐酸,生成沉淀。已知该温度下AgCl的Ksp=1.0×10-10,忽略溶液的体积变化,请计算:
①完全沉淀后,溶液中c(Ag+)=__________。 ②完全沉淀后,溶液的pH=__________。
③如果向完全沉淀后的溶液中继续加入50 mL 0.001 mol·L-1的盐酸,是否有白色沉淀生成?________________(填“是”或“否”)。
(3)在某温度下,Ksp(FeS)=6.25×10-18,该温度下,FeS的溶解度为 (该温度下溶液的密度为1g/mL)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西桂林中学高二上期中考试文化学试卷(解析版) 题型:选择题
下列化学反应的离子方程式其中正确的是( )
A.碳酸钙与盐酸反应:CO32— + 2H+ = CO2↑ + H2O
B.氨水与盐酸反应:OH—+ H+ = H2O
C.氢氧化钡溶液与硫酸反应:Ba2+ + OH—+ H+ + SO42—= BaSO4↓+ H2O
D.铁与氯化铁溶液反应:Fe + 2Fe3+ = 3Fe2+
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西桂林中学高二上期中考试理化学试卷(解析版) 题型:选择题
结构简式为 的有机物,不能发生的反应是
的有机物,不能发生的反应是
A. 消去反应 B. 加成反应 C. 酯化反应 D. 银镜反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东深圳高级中学高二上期中考试化学试卷(解析版) 题型:填空题
使用石油热裂解的副产物CH4来制取CO和H2,其生产流程如下图:
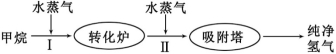
(1)工业上常利用反应Ⅰ产生的CO和H2合成可再生能源甲醇。
①已知CO(g)、CH3OH(l)的燃烧热分别为283.0 kJ·mol-1和726.5 kJ·mol-1,则CH3OH(l)不完全燃烧生成CO(g)和H2O(l)的热化学方程式为 。
(2)此流程的第I步反应为:C H4(g) + H2O(g)
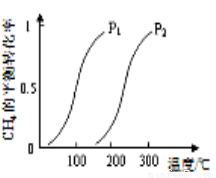
H4(g) + H2O(g) 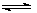 CO(g) + 3H2(g),一定条件下CH4的平衡转化率与温度、压强的关系如图。则P1_________P2。(填“<”、“>”或“=”)100℃时,将1 mol CH4和2 mol H2O通入容积为10L的恒容密闭容器中,达到平衡时CH4的转化率为0.5。此时该反应的平衡常数K=____________。
CO(g) + 3H2(g),一定条件下CH4的平衡转化率与温度、压强的关系如图。则P1_________P2。(填“<”、“>”或“=”)100℃时,将1 mol CH4和2 mol H2O通入容积为10L的恒容密闭容器中,达到平衡时CH4的转化率为0.5。此时该反应的平衡常数K=____________。
(3)此流程的第II步反应CO(g) + H2O(g) 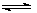 CO2(g) + H2(g),
CO2(g) + H2(g),
的平衡常数随温度的变化如下表:
温度/℃ | 400 | 500[ | 830 |
平衡常数K | 10 | 9 | 1 |
从上表可以推断:该 反应是 反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020mol/L,在该条件下,反应达到平衡时,CO的转化率为 。
反应是 反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020mol/L,在该条件下,反应达到平衡时,CO的转化率为 。
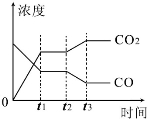
右图表示该反应在t1时刻达到平衡、在t2时刻因改变某个条件引起浓度变化的情况:图中t2时刻发生改变的条件是____(写出一种)。
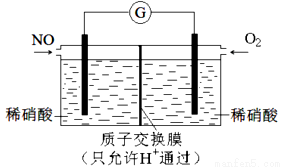
(4)某化学兴趣 小组构想将NO转化为HNO3(NO3-),装置如图,电极为多孔惰性材料。则负极的电极反应式是 。
小组构想将NO转化为HNO3(NO3-),装置如图,电极为多孔惰性材料。则负极的电极反应式是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东广州执信中学高一上期中考试化学试卷(解析版) 题型:选择题
下列反应中,离子方程式为H++OH-=H2O的是
A.CH3COOH+NaOH=CH3COONa+H2O B.HNO3+KOH=KNO3+H2O
C. 3HCl+Fe(OH)3=FeCl3+3H2O D.2HCl+Cu(OH)2=CuCl2+2H2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东广州执信中学高二上期中理化学试卷(解析版) 题型:填空题
(1)2.00g C2H2气体完全燃烧生成液态水和CO2气体,放出99.6kJ的热量,写出表示C2H2燃烧热的热化学方程式_________________________。
(2)已知下列反应的反应热:
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l)△H1=-870.3kJ/mol
②C(s)+O2(g) =CO2(g) △H2=-393.5 kJ/mol
③H2(g)+1/2O2(g)=H2O(l) △H3=-285.8kJ/mol
计算下列反应的反应热:
2C(s)+2H2(g)+O2(g)= CH3COOH(l) ΔH=____(写出计算结果)
(3)已知:
CH4(g)+ 2O2(g)= CO2 (g) + 2H2O (l) △H= -Q1 kJ/mol
2H2(g)+O2(g)= 2H2O(g) △H= -Q2 kJ/mol
2H2(g)+O2(g)= 2H2O(l) △H=- Q3 kJ/mol
取体积比4:1的甲烷和氢气的混合气体11.2L(标况),经完全燃烧恢复至常温,放出的热量为 _________。
(4)请认真观察右图,然后回答问题。

①图中反应是 (填“吸热”或“放热”)反应,该反应 (填“需要”或“不需要”)环境先提供能量。
②已知热化学方程式:H2(g)+1/2O2(g) === H2O(g) △H= -241.8kJ/mol,该反应的活化能为167.2 kJ/mol,则其逆反应的活化能为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高二12月月考化学卷(解析版) 题型:选择题
25℃ 时,向1 mL pH=1的硫酸中滴加的10 mL pH=b的NaOH溶液,形成的混合溶液成碱性则b可能为
A.10 B.11 C.12 D.13
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com