
下列排列顺序正确的是( )
①热稳定性:H2O>HF>H2S
②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HClO
④得电子能力:C<N<O<F
A.①③ B.②④
C.①④ D.②③
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
通过粮食发酵可获得某含氧有机化合物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0%。
(1)X的分子式是________________________________________________________________________。
(2)X与金属钠反应放出氢气,反应的化学方程式是__________________________(有机物用结构简式表达)。
(3)X与空气中的氧气在铜或银催化作用下反应生成Y,反应的化学方程式是________________________________________________________________________。
(4)X与高锰酸钾酸性溶液反应可生成Z,Z的名称是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应,产物的颜色按红色、红褐色、淡黄色、蓝色顺序排列的是
①金属钠在纯氧中燃烧 ②FeSO4溶液中滴入NaOH溶液并在空气中放置一段时间后 ③FeCl3溶液中滴入KSCN溶液 ④无水硫酸铜放入医用酒精中
A.③②①④ B.②③①④ C.③①②④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中能肯定金属A比金属B金属性强的是( )
A.A原子的最外层电子数比B原子的最外层电子数少
B.A原子的电子层数比B原子的电子层数多
C.1 mol A从酸中置换出H+生成的H2比1 mol B从酸中置换出H+生成的H2多
D.常温时,A能从水中置换出氢,而B不能
查看答案和解析>>
科目:高中化学 来源: 题型:
在1~18号元素中(除稀有气体元素)用元素符号或化学式填写:
(1)简单离子中,半径最小的是________。
(2)原子半径最小的是________,原子半径最大的是________。
(3)与水反应最剧烈的金属单质是________。
(4)最高价氧化物的水化物中,酸性最强的是________,碱性最强的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列与化学反应能量变化相关的叙述不正确的是( )
A.化学反应是旧键断裂和新键形成的过程
B.放热反应的反应速率总是大于吸热反应的反应速率
C.应用盖斯定律,可计算某些难以直接测量的反应焓变
D.同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH相同
查看答案和解析>>
科目:高中化学 来源: 题型:
铅蓄电池的工作原理为:Pb+PbO2+2H2SO4===2PbSO4+2H2O,研读右图,下列判断不正确的是( )
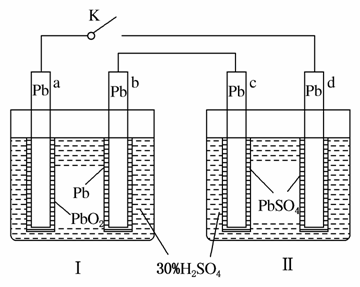
A.K闭合时,d电极反应式为:
PbSO4+2H2O-2e-===PbO2+4H++SO
B.当电路中转移0.2 mol电子时,Ⅰ中消耗的H2SO4为0.2 mol
C.K闭合时,Ⅱ中SO 向c电极迁移
向c电极迁移
D.K闭合一段时间后,Ⅱ可单独作为原电池,d电极为正极
查看答案和解析>>
科目:高中化学 来源: 题型:
25 ℃时,水的电离达到平衡:H2OH++OH- ΔH>0,下列叙述正确的是( )
A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变
C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D.将水加热,Kw增大,pH不变
查看答案和解析>>
科目:高中化学 来源: 题型:
原子序数依次递增的X、Y、Z、W是周期表中前30号元素,其中只有X、Y同周期。已知
X的最外层电子数是其内层电子数的2倍;X与Y形成的常见化合物之一常被用于高炉炼
铁;Z与X同主族,其单质在同周期元素形成的单质中熔点最高;W原子M能层为全充满
状态,且核外的未成对电子只有一个。回答下列问题:
(1)从电负性角度分析,X,Y,Z三种元素的非金属活泼性由强到弱的顺序为 。
(2)X、Y分别与H形成的化学键的极性关系为X-H Y-H(填“<”、“>”或“=”)。
(3)+l价气态基态阳离子再失去一个电子形成+2价气态基态阳离子所需要的能量称为第二
电离能I2,依次还有I3、I4、I5…,推测Z元素的电离能突增应出现在第____电离能。
(4)X的氢化物中X原子的杂化方式为sp2,则相对分子质量最小的分子式为____,
(5)W的价电子排布图为 ;下图____表示的是W晶体中微粒的堆积方式(填甲、乙或丙);若W晶体中一个晶胞的边长为a cm,则W晶体的密度为____(写出含a的表达式,用NA表示阿伏伽德罗常数)。
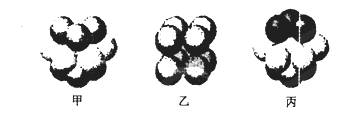
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com