
���� n��B2H6��=$\frac{13.8g}{27.6g/mol}$=0.5mol����������ȼ�գ����ɹ�̬�������������̬ˮ������ʽΪB2H6��g��+3O2��g��=B2O3��s��+3H2O��g�����ų�1016.5kJ��������Ϸ���ʽ�ɼ���1molB2H6��g��ȼ�շų���������������д�Ȼ�ѧ����ʽ����ϸ�˹���ɼ�������Һ̬ˮ�ų����������Դ˽����⣮
��� �⣺��1��n��B2H6��=$\frac{13.8g}{27.6g/mol}$=0.5mol����������ȼ�գ����ɹ�̬�������������̬ˮ������ʽΪB2H6��g��+3O2��g��=B2O3��s��+3H2O��g�����ų�1016.5kJ������1molB2H6��g��ȼ�շų�����Ϊ1016.5kJ��2=2033kJ�����Ȼ�ѧ����ʽΪB2H6��g��+3O2��g��=B2O3��s��+3H2O��g����H=-2033kJ/mol��
�ʴ�Ϊ��B2H6��g��+3O2��g��=B2O3��s��+3H2O��g����H=-2033kJ/mol��
��2����֪��H2O��1��=H2O��g����H=+44kJ•mol-1����B2H6��g��+3O2��g��=B2O3��s��+3H2O��g����H=-2033kJ/mol��
���-�١�3�ɵ�B2H6��g��+3O2��g��=B2O3��s��+3H2O��l����H=-2165kJ/mol��
���״����11.2L���������壬��0.5mol����ȫȼ������Һ̬ˮʱ�ų�������Ϊ2165kJ/mol��0.5mol=1082.5kJ��
�ʴ�Ϊ��1082.5��
���� ������Ҫ�������Ȼ�ѧ����ʽ����д��Ϊ��Ƶ���㣬���ؿ���ѧ���ķ��������ͼ�����������Ҫע����У����ʵ�״̬����Ӧ�ȵ���ֵ�뵥λ����Ӧ�ȵ���ֵ�뻯ѧ����ʽǰ���ϵ�������ȣ���Ŀ�ѶȲ���


 ѧ���쳵�����ּ��ں�����ҵϵ�д�
ѧ���쳵�����ּ��ں�����ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
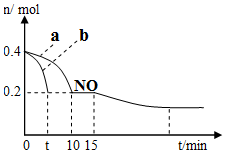 �о����֣�NOx��SO2����������Ҫ�ɷ֣���֪��
�о����֣�NOx��SO2����������Ҫ�ɷ֣���֪��| ��ѧʽ | H2CO3 | H2SO3 |
| ����ƽ�ⳣ�� | K1=4.30��10-7 K2=5.61��10-11 | K1=1.54��10-2 K2=1.02��10-7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
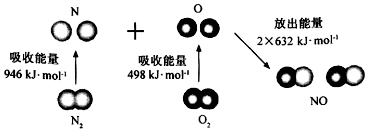
| A�� | ֱ�ۿ����÷�Ӧ�з�Ӧ�������е����������������������е������� | |
| B�� | 2 mol��̬��ԭ�ӽ������O2��g��ʱ���ܷų�498 KJ���� | |
| C�� | ����1 mol NO�����еĻ�ѧ������Ҫ����632KJ���� | |
| D�� | �÷�Ӧ���Ȼ�ѧ����ʽΪ��N2+O2�T2NO��H=+180KJ/mol�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
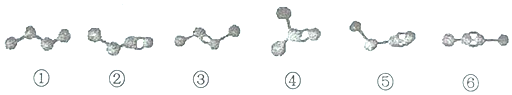
| A�� | ���ڡ��ۡ��ܵķ���ʽ��ΪC4H8������Ϊͬ���칹�� | |
| B�� | ���ݺ͢ķ���ʽ��ΪC4H6������Ϊͬ���칹�� | |
| C�� | ���ڡ��ۡ��ݡ��ֱ����������������ӳɷ�Ӧ�����ɵõ����� | |
| D�� | �����ʵ��������ں͢ݷֱ�����������ȫȼ�գ��������ĵ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | v��CO��=0.03mol•L-1•s-1 | B�� | v��NO2��=0.7mol•L-1•min-1 | ||
| C�� | v��N2��=0.4mol•L-1•min-1 | D�� | v��CO2��=1.1mol•L-1•min-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| 2 | �� | �� | ||||||
| 3 | �� | �� | �� | �� | �� | �� | �� |
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Ϊ8�ĵ�ԭ�ӣ�${\;}_{8}^{15}$N | |
| B�� | ������ĵ���ʽ��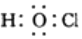 | |
| C�� | PCl5���ӵ�ÿ��ԭ�Ӷ�����8�����ȶ��ṹ | |
| D�� | �õ���ʽ��ʾNaCl���γɹ��̣�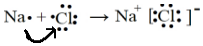 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������Һ�м���Na2SO4��ʹ����� | |
| B�� | ����ˮ�����ɻ�Ϊͬ���칹��������Ǻ��� | |
| C�� | ˳-2һ��ϩ�ͷ�-2-��ϩ�ļ�����ﲻͬ | |
| D�� | ʯ�͵ķ����ú����������ڻ�ѧ�仯 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com