
煤的气化可以减少环境污染,而且生成的CO和H2被称作合成气,能合成很多基础有机化工原料。
(1)工业上可利用CO生产乙醇:2CO(g)+4H2(g) CH3CH2OH(g)+H2O(g) ΔH1
CH3CH2OH(g)+H2O(g) ΔH1
又知:H2O(l)=H2O(g) ΔH2
CO(g)+H2O(g) CO2(g)+H2(g) ΔH3
CO2(g)+H2(g) ΔH3
工业上也可利用CO2(g)与H2(g)为原料合成乙醇:
2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(l) ΔH
CH3CH2OH(g)+3H2O(l) ΔH
则ΔH与ΔH1、ΔH2、ΔH3之间的关系是ΔH=____________。
(2)一定条件下,H2、CO在体积固定的绝热密闭容器中发生如下反应:4H2(g)+2CO(g) CH3OCH3(g)+H2O(g),下列选项不能判断该反应达到平衡状态的是__________。
CH3OCH3(g)+H2O(g),下列选项不能判断该反应达到平衡状态的是__________。
A.v(H2)正=2v(CO)逆 B.平衡常数K不再随时间而变化
C.混合气体的密度保持不变 D.CH3OCH3和H2O的体积之比不随时间而变化
(3)工业可采用CO与H2反应合成再生 能源甲醇,反应:CO(g)+2H2(g)
能源甲醇,反应:CO(g)+2H2(g) CH3OH(g),在一容积可变的密闭容器中充有10 mol CO和20 mol H2,在催化剂作用下发生反应生成甲醇,CO的平衡转化率(α)与温度(T)、压强(p)的关系如图1所示。
CH3OH(g),在一容积可变的密闭容器中充有10 mol CO和20 mol H2,在催化剂作用下发生反应生成甲醇,CO的平衡转化率(α)与温度(T)、压强(p)的关系如图1所示。
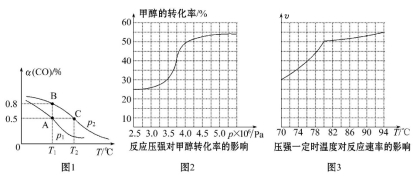
①合成甲醇的反应为______________(填“放热”或“吸热”)反应。
②A、B、C三点的平衡常数KA、KB、KC的大小关系为____________________。p1和p2的大小关系为___________。
③若达到平衡状态A时,容器的体积为10 L,则在平衡状态B时容器的体积为________L。
(4)工业上可通过甲醇羰基化法制取甲酸甲酯,其反应的热化学方程式为CH3OH(g)+CO(g) HCOOCH3(g) ΔH2=-29.1 kJ·mol-1。科研人员对该反应进行了研究,部分研究结果如图2、3:
HCOOCH3(g) ΔH2=-29.1 kJ·mol-1。科研人员对该反应进行了研究,部分研究结果如图2、3:
①从反应压强对甲醇转化率的影响“效率”看,工业制取甲酸甲酯应选择的压强是________(填“3.5×106Pa”“4.0×106Pa”或“5.0×106Pa”)。
②实际工业生产中采用的温度是80℃,其理由是___________________。
科目:高中化学 来源:2016-2017学年辽宁省分校高一上期中化学卷(解析版) 题型:选择题
某溶液中只含有Na+、Al3+、Cl-、SO42-四种离子,已知前三种离子的个数比3:2:1,则溶液中Al3+和SO42-的个数比 为
为
A.1:2 B.1:4 C.3:4 D.3:2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北冀州中学高一12月月考文化学卷(解析版) 题型:选择题
下列离子方程式书写正确的是( )
A.铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑
B.AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓
C.三氯化铁溶液中加入铁粉Fe3++Fe=2Fe2+
D.FeCl2溶液跟Cl2反应:2Fe2++Cl2=2Fe3++2Cl-
查看答案和解析>>
科目:高中化学 来源:2017四川省自贡市高三第一次诊断考试化学试卷(解析版) 题型:填空题
已知二元酸H2A在水中存在以下电离:H2A==H++HA-,HA- H++A2-,回答下列问题:
H++A2-,回答下列问题:
(1)Na2A溶液呈________性,理由是___________(用离子方程式表示)。
(2)NaHA溶液呈________性,理由是___________。
(3)0.1mol/L的NaHA溶液的PH=3,则Ka(HA-)=_____________。
(4)某温度下,向10 mL 0.1 mol/L NaHA溶液中加入0.1 mol/L KOH溶液V mL至溶液中水的离子积常数Ka=c2(OH-),此时溶液呈___________性,V____________10 (填“<”“>”或“=”)c(K+)/c(Na+) ____________1(填“<”“>”或“=”),溶液中电荷守恒等式为____________。
查看答案和解析>>
科目:高中化学 来源:2017四川省自贡市高三第一次诊断考试化学试卷(解析版) 题型:选择题
氢镍电池是近年开发出来的可充电电池,它可以取代会产生污染的铜镍电池。氢镍电池的总反应式是:
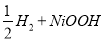
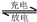
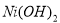 据此反应式判断,下列叙述中不正确的是
据此反应式判断,下列叙述中不正确的是
A. 电池放电时,电池负极周围溶液的PH不断增大
B. 电池放电时,正极的电极反应为: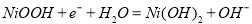
C. 电池充电时,阳极周围溶液的的PH不断减小
D. 电池充电时,阴极的电极反应为:2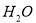 +2
+2
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省大连市高三12月月考化学试卷(解析版) 题型:选择题
某溶液中含有如下离子组中的若干种:K+、Mg2+、Fe3+、Fe2+、CO32-、NO3-、SO42-、I-、SiO32-、Cl-,且物质的量浓度相同。某同学欲探究该溶液的组成,进行了如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到浅紫色火焰;
Ⅱ.另取原溶液加入足量盐酸有无色气体生成,该气体遇空气变成红棕色,此时溶液颜色加深,但无沉淀生成;
Ⅲ.取Ⅱ反应后的溶液分置于两支试管中,第一支试管中加入BaCl2溶液,有白色沉淀生成,再滴加KSCN溶液上层清液变红;第二支试管中加入CCl4,充分振荡静置后溶液分层,下层出现紫红色。下列说法正确的是( )
A.原溶液中肯定不含Mg2+、SiO32-
B.步骤Ⅱ中无色气体可能含有CO2,原溶液中可能含有CO32-
C.原溶液由K+、Fe2+、NO3-、I-、SO42-五种离子组成
D.原溶液中一定含有Mg2+、Cl-
查看答案和解析>>
科目:高中化学 来源:2017届江西省等四校高三上联考一化学试卷(解析版) 题型:选择题
X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如下转化关系(其他产物已略去):
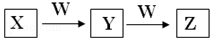
下列说法不正确的是
A.若W是单质铁,则Z溶液可能是FeCl2溶液
B.若W是盐酸,则X与Z可反应生成Y
C.若X是FeCl3溶液,则W可以是Zn或Al
D.若W是硝酸溶液, 则X与Z不能反应生成Y
查看答案和解析>>
科目:高中化学 来源:2017届江西省赣州市十三县(市)高三上期中化学试卷(解析版) 题型:推断题
置换反应是中学化学中常见的反应类型,其的通式可表示为:
单质甲+化合物A=单质乙+化合物B
单质甲、乙和化合物A、B为中学常见物质,请回答下列问题:
(1)若单质乙为空气中的一种主要成分,则该反应的化学方程式为 。
(2)若单质甲和化合物B均具有铁磁性,则该反应的化学方程式为 。
(3)若化合物A是红棕色粉末状固体,化合物B具有两性,则该反应的化学方程式为 。
(4)若单质乙是做光伏电池组件的重要材料,写出该反应的化学方程式 。
(5)若单质甲是金属,化合物A为一种温室效应气体,则该反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高一上月考三化学试卷(解析版) 题型:选择题
在食品中的一些元素含量 偏高会引起毒性反应,食品卫生法对它们
偏高会引起毒性反应,食品卫生法对它们 的含量最高标准有极严格规定,这些元素是
的含量最高标准有极严格规定,这些元素是
① Na ②Mg ③As砷 ④Cd镉 ⑤Ca ⑥Zn ⑦Hg ⑧Pb ⑨Cu ⑩K中的
Na ②Mg ③As砷 ④Cd镉 ⑤Ca ⑥Zn ⑦Hg ⑧Pb ⑨Cu ⑩K中的
A.②④⑥⑦⑧ B.②④⑥⑧⑨
C.⑥⑦⑧⑨⑩ D.③④⑦⑧⑨
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com