
X��Y��Z��L��M��N����Ԫ�ص�ԭ��������������X��Y��Z��L����ɵ����ʵĻ���Ԫ�أ�M�ǵؿ��к�����ߵĽ���Ԫ�ء��ش��������⣺
��1��L��ԭ�ӽṹʾ��ͼΪ ��M��Ԫ�����ڱ��е�λ��Ϊ ��ǰ����Ԫ�ص�ԭ�Ӱ뾶�Ӵ�С��˳���� ����Ԫ�ط��ű�ʾ����Z��L��Ԫ�صĵ�һ�����ܴ�С��ϵΪ�� �� ����дԪ�ط��ţ���ԭ���� ��
��2��Z��X��Ԫ�ذ�ԭ����Ŀ��l��3��2��4���ɷ���A��B��A�ķ��ӹ���Ϊ ��B�ĽṹʽΪ ��
��3��N������������Ԫ�أ���Lͬһ���壬Nԭ�ӱ�Lԭ�Ӷ��������Ӳ㣬��N�ĵ����Ų�ʽΪ ��������������Ӧ��ˮ���ﻯѧʽΪ ������2 ~ 5����Ԫ�ص��ʷֱ���H2��Ӧ����l mol��̬�⻯��ķ�Ӧ�����£���ʾ����1mol H2N��Ӧ�ȵ���__________������ĸ���ţ���
A��+99��7 mol��L��1 B��+29��7 mol��L��1
C����20��6 mol��L��1 D����241��8 kJ��mol��1
��4����M������������ʯī��������NaHCO3��Һ�����Һ���е�⣬����������R��R���ȷֽ����ɻ�����Q��д����������R�ĵ缫��Ӧʽ�� ����R����Q�Ļ�ѧ����ʽ�� ��
��1��O��![]() ��1�֣�����3���ڵڢ�A�壨1�֣���Al > C > N > O > H ��2�֣���N��1�֣� ��O��1�֣� ��Nԭ�����������Ӵ��ڰ����״̬���Ƚ��ȶ�����2�֣�
��1�֣�����3���ڵڢ�A�壨1�֣���Al > C > N > O > H ��2�֣���N��1�֣� ��O��1�֣� ��Nԭ�����������Ӵ��ڰ����״̬���Ƚ��ȶ�����2�֣�
��2�������� ��1�֣� ![]() ��1�֣�
��1�֣�
��3��1s22s22p63s23p63d104s24p4��[Ar] 3d104s24p4 ��2�֣��� H2SeO4��1�֣���B��1�֣�
��4��Al+3HCO3����3e����Al��OH��3��+3CO2��[��Al��3e����Al3+��Al3++3HCO3����Al��OH��3��+3CO2��]
��2�֣���2Al��OH��3![]() Al2O3 + 2H2O ��2�֣� ��
Al2O3 + 2H2O ��2�֣� ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�



| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
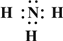
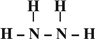
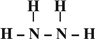
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com