
【题目】一定温度下在体积为5 L的密闭容器中发生可逆反应。(Ⅰ)若某可逆反应的化学平衡常数表达式为:K=![]()
(1)写出该反应的化学方程式:
(2)能判断该反应一定达到化学平衡状态的依据是 (填选项编号)。
A.容器中气体的平均相对分子质量不随时间而变化
B.v正(H2O)=v逆(H2)
C.容器中气体的密度不随时间而变化
D.容器中总质量不随时间而变化
E.消耗n mol H2的同时消耗n mol CO
(Ⅱ)若该密闭容器中加入的是2 mol Fe(s)与1 mol H2O(g),t1秒时,H2的物质的量为0.20 mol,到第t2秒时恰好达到平衡,此时H2的物质的量为0.35 mol。
(1)t1~t2这段时间内的化学反应速率v(H2)= 。
(2)若继续加入2 mol Fe(s),则平衡 移动(填“向正反应方向”、“向逆反应方向”或“不”),继续通入1 mol H2O(g),再次达到平衡后,H2物质的量为 mol。
(3)该反应的逆反应速率随时间变化的关系如图。t1时改变了某种条件,改变的条件可能是 、 (填写2项)。

【答案】 (Ⅰ)(1)C(s)+H2O(g)![]() CO(g)+H2 (g)
CO(g)+H2 (g)
(2)A、B、C (Ⅱ)(1)0.03/(t2-t1)mol·L-1·s-1
(2)不 0.7
(3)使用了催化剂 增大了H2的浓度
综合演练
【解析】(Ⅰ)(1)根据化学平衡常数的定义,找出反应物、生成物以及系数,写出方程式C(s)+H2O(g)![]() CO(g)+H2 (g)。
CO(g)+H2 (g)。
(2)由于C是固体,因此随着反应的进行,容器中气体的平均相对分子质量随着时间而变化,A正确; v正(H2O)=v逆(H2),说明正、逆反应速率相等,B对;由于C是固体,因此随着反应的进行,容器中气体的质量随着时间而变化,而体积不变,因此密度随时间而变化,而总质量一直不发生变化,所以C可作为判断平衡的标志,而D不能。消耗n mol H2的同时消耗n mol CO均为逆反应速率,不能判断该反应一定达到化学平衡状态。
(Ⅱ)(1)v(H2)=(0.35-0.20) mol/5 L·(t2-t1)=0.03/(t2-t1) mol·L-1·s-1。
(2)Fe为固体,加入2 mol Fe,则平衡不移动。再通入1 mol H2O(g),相当于在原来通入1 mol H2O(g)的基础上浓度加倍,相当于加压,但由于该反应前后气体体积不变,所以相对于通入1 mol H2O(g)时处于相同的平衡状态,但各物质的浓度是原来的2倍,所以n(H2)=0.7 mol。
(3)使用催化剂、增大H2的浓度均可提高逆反应速率。


科目:高中化学 来源: 题型:
【题目】在高锰酸钾固体上滴加浓盐酸,马上产生黄绿色气体。反应的化学方程式为:2KMnO4 + 16HC1=2KC1 + 2MnCl2 + 5C12↑+ 8H2O
回答下列问题:
(1)此反应中的氧化剂是____,当在标准状况下产生0.112L氯气,转移的电子数为____mol。
(2)氯原子的核电荷数为______;氧原子的原子结构示意图_______ 。
(3)在KC1固体中存在的化学键是__________;写出H2O电子式_________。
(4)工业上用氯气与消石灰作原料制造漂粉精,此反应的化学方程式是_________。
(5)浓盐酸的溶质是氯化氢,用一个实验证明氯化氢极易溶于水。_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是
A. 碳酸钠的水解反应: CO32-+ H2O → HCO3—+ OH-
B. 氢氧化钡溶液中滴加硫酸:Ba2++SO42-→ BaSO4↓
C. 硫酸铁溶液中加入铁钉:Fe3++Fe → 2Fe2+
D. 碳酸氢钙溶液中加入过量的NaOH溶液:Ca2++2HCO3-+2OH-→CaCO3↓+2H2O+ CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示。A、B、C、E为气体,其中A能使湿润的红色石蕊试纸变蓝,B为无色单质,E是为红棕色。G是紫红色金属单质,H的水溶液为蓝色。
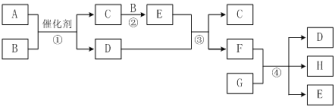
⑴A的电子式为______。
⑵写出反应①的化学方程式:______。
⑶写出反应③的化学方程式:______。该方程式中转移的电子数目为______个。
⑷写出反应④的离子方程式:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下:
元素 | 相关信息 |
A | 基态原子的价电子排布式为nSnnPn |
B | 元素原子的核外p电子数比s电子数少1个 |
C | 最外层电子数是电子层数的3倍 |
D | 简单离子是第三周期元素中离子半径最小的 |
E | 价电子层中的未成对电子数为4 |
请回答下列问题:
(1)写出下列元素符号:A______, B_______,C________,D__________。
(2)写出C元素在周期表的位置_________,E2+价电子的轨道表示式______________,B元素能量最高的电子为____轨道上的电子,其轨道呈______形。
(3)按原子轨道的重叠方式,1molA与C形成的最高价化合物中σ键有______个,π键有______个。(阿伏加德罗常数的值用NA表示)
(4)B、C、D的简单离子的半径由大到小的顺序为________(用离子符号表示)。
(5)写出C的核外有18个电子的氢化物的电子式_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】糖类、油脂、蛋白质是重要的营养物质,下列说法正确的是( )
A.棉、麻、蚕丝都是纤维素B.油脂为混合物
C.1 mol 蔗糖完全水解可得 2 mol 葡萄糖D.遇 Pb2+凝固后的鸡蛋清可溶于蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cl2与NaOH溶液反应可生成NaCl、NaClO和NaClO3(Cl-和ClO-)的比值与反应的温度有关,用24gNaOH配成的250mL溶液,与Cl2恰好完全反应(忽略Cl2与水的反应、盐类的水解及溶液体积变化):
(1)NaOH溶液的物质的量浓度_____mol·L-1;
(2)某温度下,反应后溶液中c(Cl-)=6c(ClO-),则溶液中c(ClO-) =_____mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中,A、B、C、D、E、F、G均为有机化合物。
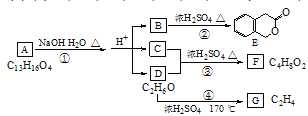
根据上图回答问题:
(1)D、F的化学名称是________、________。
(2)写出下列反应的化学方程式,并注明反应类型。
②____________________________________________,________;
④____________________________________________,________;
(3)A的结构简式是__________________,1 mol A与足量的NaOH溶液反应会消耗________mol NaOH。
(4)写出符合下列3个条件的B的同分异构体____________________。
①含有邻二取代苯环结构②与B有相同官能团③不与FeCl3溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1.92gCu放入50mL2mol/L稀硝酸中,当铜全部溶解后,
(1)产生的气体是____________,标准状况下的体积是___________L;
(2)溶液中H+物质的量浓度是______________mol/L,NO3- 物质的量浓度是______mol/L(溶液体积变化忽略不计)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com