
| A. | 惰性电极电解氯化钾溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| B. | 能溶解Fe(OH)3的溶液中含有:HCO3-、Na+、Mg2+、Cl- | |
| C. | 中性溶液中可能大量存在Fe3+、K+、Cl-、SO42- | |
| D. | 石灰乳与Na2CO3溶液混合:Ca2++CO32-=CaCO3↓ |
分析 A.惰性电极电解氯化钾溶液,阴极氢离子得到电子生成氢气,阳极氯离子放电生成氯气;
B.能够溶解氢氧化铁的溶液中存在大量氢离子,碳酸氢根离子能够与氢离子反应;
C.铁离子部分水解,溶液显示酸性,不可能为中性;
D.石灰乳中,氢氧化钙不能拆开,应该两边化学式.
解答 解:A.用惰性电极电解氯化钾溶液,反应生成氯气、氢气和氢氧化钾,反应的离子方程式为:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH-,故A正确;
B.能溶解Fe(OH)3的溶液中含有大量氢离子,HCO3-与氢离子反应,在溶液中不能大量共存,故B错误;
C.Fe3+在溶液中部分水解,溶液显示酸性,不可能为中性溶液,故C错误;
D.石灰乳与碳酸钠反应生成碳酸钙和氢氧化钠,氢氧化钙不能拆开,正确的离子方程式为:Ca(OH)2+CO32-=CaCO3↓+2OH-,故D错误;
故选A.
点评 本题考查了离子方程式的书写判断,题目难度中等,注意掌握离子方程式的书写原则,明确电解原理及电极反应式的书写方法,D为易错点,石灰乳中的氢氧化钙在离子方程式中不能拆开.


科目:高中化学 来源: 题型:选择题
| A. | 生物质能来源于植物及其加工产品所贮存的能量,绿色植物通过光合作用将化学能转化为生物质能 | |
| B. | 用氨水法处理燃煤烟气中的二氧化硫,即可消除其污染,又可得到副产品硫酸铵 | |
| C. | 某小组研究人员成功制备出了四氧化铱正离子(IrO4+),其球棍模型为 ,由此可判断其中铱元素显+9价 ,由此可判断其中铱元素显+9价 | |
| D. | 门捷列夫根据元素性质随元素的相对原子质量递增而显现元素周期性变化的规律排出了第一张元素周期表 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 有A、B、C、D、E五种短周期元素,A、C同周期,B、D同主族,E是五种元素中原子半径最小的元素.A是构成矿物和岩石的主要成分的元素,C、D可生成离子化合物C3D2.A的单质与E的单质在常温下就可发生反应,生成化合物F.据此回答下列问题:
有A、B、C、D、E五种短周期元素,A、C同周期,B、D同主族,E是五种元素中原子半径最小的元素.A是构成矿物和岩石的主要成分的元素,C、D可生成离子化合物C3D2.A的单质与E的单质在常温下就可发生反应,生成化合物F.据此回答下列问题: ;A单质及其最高价氧化物均属于原子晶体(填晶体类型)
;A单质及其最高价氧化物均属于原子晶体(填晶体类型)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
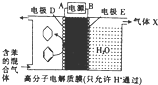 一定条件下,利用如图所示装置可实现有机物的储氢,下列有关说法正确的是( )
一定条件下,利用如图所示装置可实现有机物的储氢,下列有关说法正确的是( )| A. | A为电源的正极 | |
| B. | 气体X为H2 | |
| C. | 电极E为阴极 | |
| D. | 电极D的电极反应式为C6H6+6H++6e-=C6H12 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 化学反应 | 离子方程式 | 评价 |
| A | NaClO溶液中通入过量SO2气体 | ClO-+H2O+SO2═HClO+HSO3- | 正确 |
| B | NH4HSO3溶液中加入等量NaOH | HSO3-+OH-═SO32-+H2O | 错误,OH-能同时与NH4+、HSO3-反应 |
| C | Na2CO3 的水解 | CO32-+H2O?CO2↑+2OH- | 错误,水解反应不加气体符号 |
| D | 用稀硝酸清洗做过银镜反应的试管 | Ag+4H++NO3-═Ag++NO↑+2H2O | 错误,等式两端电荷不守恒 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由SO2制亚硫酸钠:SO2$\stackrel{Na_{2}CO_{3}溶液}{→}$NaHSO3溶液$→_{调节溶液的pH}^{NaOH溶液}$Na2SO3溶液 | |
| B. | 由NaCl制漂白粉精:NaCl(aq)$\stackrel{电解}{→}$Cl2$\stackrel{澄清石灰水}{→}$漂粉精 | |
| C. | 由NH3制硝酸:NH3$\stackrel{O_{2}}{→}$NO2$\stackrel{H_{2}O}{→}$HNO3 | |
| D. | 由乙烯制乙酸:H2C=CH2$→_{催化剂}^{H_{2}O}$CH3CH2OH$→_{△}^{CuO_{2}}$CH3CHO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中,K+、Fe2+、C6H5OH、Br-可以大量共存 | |
| B. | 和KI溶液反应的离子方程式:2Fe3++2I-=2Fe2++I2 | |
| C. | 和Ba(OH)2溶液反应的离子方程式:Fe3++SO42-+Ba2++3OH-=Fe(OH)3↓+BaSO4↓ | |
| D. | 1L0.1mol/L该溶液和足量的Ca充分反应,生成11.2gFe |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素X与氢形成的原子比为1:1的化合物有很多种 | |
| B. | 元素W、X的氯化物中,各原子均满足8电子的稳定结构 | |
| C. | 元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成 | |
| D. | 元素Z可与元素X形成共价化合物XZ2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com