
将黑色的Fe2S3固体加入足量盐酸中,溶液中有淡黄色固体生成,产物还有____、______。过滤,微热滤液,然后加入过量的氢氧化钠溶液,可观察到的现象是______________。
科目:高中化学 来源: 题型:
金刚石和石墨均为碳的同素异形体,它们燃烧时,若氧气不足生成一氧化碳,若充分燃烧生成二氧化碳,反应中放出的热量如图所示。
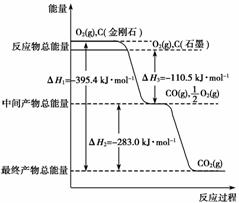
(1)等质量的金刚石和石墨完全燃烧,________(填“金刚石”或“石墨”)放出的热量更多,写出表示石墨燃烧热的热化学方程式:___________________________________。
(2)在通常状况下,________(填“金刚石”或“石墨”)更稳定,写出石墨转化为金刚石 的热化学方程式:__________________________________________________________
________________________。
(3)12 g石墨在一定量空气中燃烧,生成气体36 g,该过程中放出的热量为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有机化学反应因条件不同,可生成不同的产物.例如:
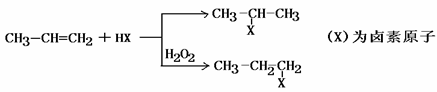
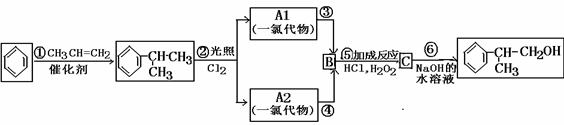
请回答下列问题:
(1) 反应①的反应类型:_________;
(2)写出A1、A2可能的结构简式: _____________, ________ ;
(3)B的结构简式:_____________ C的结构简式:______ ;
(4) 与D的碳架结构相同且含有羟基的同分异构体有 _种(不包括D).任意写出其中一种_____________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
含有砒霜(As2O3)的试样和锌、盐酸混合反应,生成的砷化氢(AsH3)在热玻璃管中完全分解成单质砷和氢气。若砷的质量为1.50mg,则
A.被氧化的砒霜为1.98mg
B.分解产生的氢气为0.672ml
C.和砒霜反应的锌为3.90mg
D.转移的电子总数为6×10―5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨工艺的一个重要工序是铜洗,其目的是用铜液[醋酸二氨合铜(I)、氨水]吸收在生产过程中产生的CO和CO2等气体。铜液吸收CO的反应是放热反应,其反应方程式为:
Cu(NH3)2Ac+CO+NH3 [Cu(NH3)3CO]Ac
[Cu(NH3)3CO]Ac
完成下列填空:
1.如果要提高上述反应的反应速率,可以采取的措施是_________。(选填编号)
a.减压 b.增加NH3的浓度 c.升温 d.及时移走产物
2.铜液中的氨可吸收二氧化碳,写出该反应的化学方程式。
_________________________________________
3.简述铜液吸收CO及铜液再生的操作步骤(注明吸收和再生的条件)。
__________________________________________
4.铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为____________________。其中氮元素原子最外层电子排布的轨道表达式是_________________________。通过比较_____________可判断氮、磷两种非金属元素的非金属性强弱。
5.已知CS2与CO2分子结构相似,CS2的电子式是____________。CS2熔点高于CO2,其原因是__________。
硫在自然界中以游离态和多种化合态形成出现。硫的化合物大多具有氧化性或还原性。
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上用电石-乙炔法生产乙烯的反应如下:
CaO+3C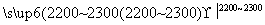 CaC2+CO
CaC2+CO
CaC2+2H2O→HC≡CH↑+Ca(OH)2
HC≡CH↑+HCl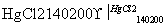 CH2=CHCl
CH2=CHCl
电石-乙炔法的优点是流程简单,产品纯度高,而且不依赖于石油资源。
电石-乙炔法的缺点是___________________、_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于有机物的叙述正确的是
A.棉花和合成纤维的主要成分都是纤维素
B.蛋白质溶液中加入浓的硫酸铵溶液会发生变性
C.乙酸乙酯中混有的乙酸杂质可以用饱和碳酸钠溶液除去
 D.由
D.由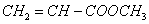 合成的聚合物为
合成的聚合物为 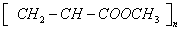
查看答案和解析>>
科目:高中化学 来源: 题型:
酸性高锰酸钾溶液能将醇氧化成一系列产物,反应中KMnO4中的Mn被还原为Mn2+,用0.2 mol·L-1的酸性高锰酸钾溶液滴定20.0 mL 0.25 mol·L-1的乙二醇溶液,当用去20.0 mL酸性高锰酸钾溶液时,再滴加半滴酸性高锰酸钾溶液时刚好呈紫色,振荡且半分钟内不退色,则乙二醇被氧化的产物是( )。
A.HO—CH2—CHO B.OHC—CHO
C.HOOC—CHO D.CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
LiSOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4SOCl2。电池的总反应可表示为4Li+2SOCl2===4LiCl+S+SO2↑。
请回答下列问题:
(1)电池的负极材料为__________,发生的电极反应为__________________________
________________。
(2)电池正极发生的电极反应为_________________________________________ ___。
___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com