
 A、B、M、D、E是原子序数依次增大的五种短周期元素.A元素的一种原子中不含中子.B、M、D、E分别在下表(周期表的一部分)不同的空格内占有相应的位置,E的原子序数是D的原子序数的2倍.试回答:
A、B、M、D、E是原子序数依次增大的五种短周期元素.A元素的一种原子中不含中子.B、M、D、E分别在下表(周期表的一部分)不同的空格内占有相应的位置,E的原子序数是D的原子序数的2倍.试回答: ,E的原子序数是D的原子序数的2倍,则D为O元素、E为S元素、M为N元素、B为C元素,即:A为H、B为C、M为N、D为O、E为S元素,据此进行解答.
,E的原子序数是D的原子序数的2倍,则D为O元素、E为S元素、M为N元素、B为C元素,即:A为H、B为C、M为N、D为O、E为S元素,据此进行解答. ,E的原子序数是D的原子序数的2倍,则D为O元素、E为S元素、M为N元素、B为C元素,即:A为H、B为C、M为N、D为O、E为S元素,
,E的原子序数是D的原子序数的2倍,则D为O元素、E为S元素、M为N元素、B为C元素,即:A为H、B为C、M为N、D为O、E为S元素,

 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:
| A、用盐酸除去BaSO4中混有的少量BaCO3 漏斗,烧杯、玻璃棒、胶头滴管、滤纸 |
| B、从食盐水中获得NaCl晶体酒精灯、玻璃棒、坩埚、泥三角 |
| C、用0.l0mol?L-1的盐酸测定未知浓度的NaOH溶液 碱式滴定管、酸式滴定管、锥形瓶、烧杯 |
| D、用溴水和CCl4除去NaBr溶液中少量NaI 烧杯、玻璃棒、胶头滴管、分液漏斗 |
查看答案和解析>>
科目:高中化学 来源: 题型:
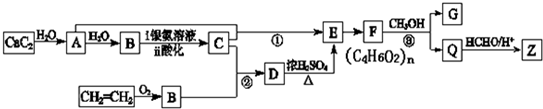
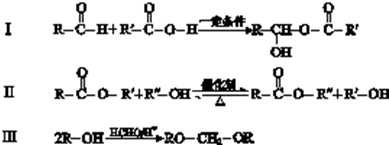
查看答案和解析>>
科目:高中化学 来源: 题型:

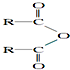
| H2O |
| LiAlH4 |
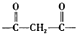 .
.查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
 (NaN3)是汽车安全气囊中的主要成分,能在发生碰撞的瞬间分解产生大量气体将气囊鼓起.实验室测定叠氮化钠样品中NaN3的质量分数.实验步骤如下:
(NaN3)是汽车安全气囊中的主要成分,能在发生碰撞的瞬间分解产生大量气体将气囊鼓起.实验室测定叠氮化钠样品中NaN3的质量分数.实验步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
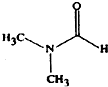 淮南市煤炭年产量已达到1忆吨以上,是我国13个忆吨煤炭生产基地之一.二甲基甲酰胺(C3H7NO)是以煤炭为原料的重要化工产品之一,其结构如图所示,下列关于二甲基甲酰胺的说法不正确的是( )
淮南市煤炭年产量已达到1忆吨以上,是我国13个忆吨煤炭生产基地之一.二甲基甲酰胺(C3H7NO)是以煤炭为原料的重要化工产品之一,其结构如图所示,下列关于二甲基甲酰胺的说法不正确的是( )| A、元素电负性大小为:O>N>C |
| B、B二甲基甲酰胺分子中既含有极性键又含有非极性键 |
| C、二甲基酰胺具有还原性,在化学反应中长做还原剂 |
| D、在空气中完全燃烧73g二甲基甲酰胺可以得到标准状况下67.2LCO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碘是人体必需的微量元素,所以要多吃富含高碘酸的食物 |
| B、为了增加食物的营养成分,可以大量使用食品添加剂 |
| C、聚乙烯塑料的老化是由于发生了加成反应 |
| D、粮食酒主要经过了淀粉→葡萄糖→乙醇的化学变化过程 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com