
 ��
������ ��1�����ݻ�������Ԫ�ػ��ϼ۴�����Ϊ0���㣬��Ԫ�ػ��ϼ�+1�ۣ���Ԫ�ػ��ϼ�-2�ۣ�CN-�����к���̼������������1����λ����ɣ�CN-��̼ԭ������8�����ȶ��ṹ��
��2������Ԫ���غ��֪�������̿��������Ӧ��ȡ NaCN��ͬʱ������ˮ��
��3���軯����Һ��CN-��˫��ˮ����ΪHCO3-��ͬʱ�ų�NH3����ClO2 ����й©���軯�ƣ�NaCN�����õ�����NaCl��N2 ��CO2���÷�Ӧ��ClԪ�ػ��ϼ���+4�۱�Ϊ-1�ۡ�NԪ�ػ��ϼ���-3�۱�Ϊ0�ۣ�CԪ�ػ��ϼ���+2�۱�Ϊ+4�ۣ�����ת�Ƶ����غ���ƽ����ʽ���ٸ����������ƺͶ������ȵĹ�ϵʽ���㣮
��� �⣺��1��NaCN����Ԫ�ػ��ϼ�+1�ۣ���Ԫ�ػ��ϼ�-3�ۣ��ϼ۴�����Ϊ0���㣬+1+x-3=0��x=+2��CN-�����к���̼������������1����λ����ɣ������ʽΪ�� ��
��
�ʴ�Ϊ��+2�� ��
��
��2������Ԫ���غ��֪�������̿��������Ӧ��ȡ NaCN��ͬʱ������ˮ����Ӧ�Ļ�ѧ����ʽΪ��Na2CO3+C+2NH3$\frac{\underline{\;����\;}}{\;}$2NaCN+3H2O��
�ʴ�Ϊ��Na2CO3+C+2NH3$\frac{\underline{\;����\;}}{\;}$2NaCN+3H2O��
��3����������Ϊ�������軯����Һ��CN-��˫��ˮ����ΪHCO3-��ͬʱ�ų�NH3����Ӧ�Ļ�ѧ����ʽΪ��NaCN+H2O2+H2O=NaHCO3+NH3�������ӷ���ʽΪ��CN-+H2O2+H2O�TNH3��+HCO3-����ClO2 ����й©���軯�ƣ�NaCN�����õ�����NaCl��N2 ��CO2���÷�Ӧ��ClԪ�ػ��ϼ���+4�۱�Ϊ-1�ۡ�NԪ�ػ��ϼ���-3�۱�Ϊ0�ۣ�CԪ�ػ��ϼ���+2�۱�Ϊ+4�ۣ�����ת�Ƶ����غ���ƽ����ʽ2ClO2+2NaCN=2NaCl+N2+2CO2��n��NaCN��=4��10-5mol•L-1��1000L=0.04mol�����ݷ���ʽ֪�����Ķ����������ʵ���Ϊ0.04mol��������=0.04mol��67.5g/mol=2.7g��
�ʴ�Ϊ��CN-+H2O2+H2O�TNH3��+HCO3-��2.7��
���� ���⿼�黯ѧ������д��������ԭ��֪ʶ��Ϊ�߿��������ͺ�Ƶ���㣬������ѧ���ķ��������ͼ��������Ŀ��飬����������ԭ��Ӧ����ʽ����д����ȷ������ԭ��Ӧ��ʧ�����غ�����ǽ��ؼ�����Ŀ�Ѷ��еȣ�


 �γ̴����Ծ�����100��ϵ�д�
�γ̴����Ծ�����100��ϵ�д� �¾�����ĩ���100��ϵ�д�
�¾�����ĩ���100��ϵ�д� ȫ�ܴ���100��ϵ�д�
ȫ�ܴ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
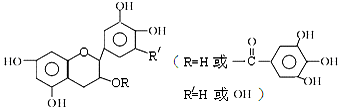
| A�� | ����������FeCl3��Һ������ɫ��Ӧ | |
| B�� | 1mol������������10mol NaOH��Ӧ | |
| C�� | �����£������ز�����ˮ��Ҳ�������л��ܼ� | |
| D�� | ������һ�����ܷ���ˮ�ⷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ƹ�ҵ��ˮ���ŷ� | B�� | �Ժ�ˮ������������ | ||
| C�� | ����ũ����ˮ | D�� | ������ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��H1����H3 | B�� | ��H3=��Hl+��H2 | ||
| C�� | ��Ӧ�ٵĻ��Ϊ24.4 kJ•mol-1 | D�� | ��Ӧ��һ�������Է����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮϡ��ʱ����$\frac{c��O{H}^{-}��}{C��{H}^{+}��}$��ֵ�������Һ�пɴ������ڣ�MnO4-��CO32-��K+��NH4+ | |
| B�� | 100��ʱ����pH=2��������Һ��pH=12������������Һ�������ϣ���Һ������ | |
| C�� | 25��ʱ��NaB��Һ��pH=9����c��Na+ ��-c��B-��=9.9��10-6mol•L-1 | |
| D�� | ��0.2mol•L-1 ��һԪ����HA��Һ��0.1mol•L-1 ��NaOH��Һ�������ϣ�2c��OH-��+c��A-��=2c��H+��+c��HA�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڢ� | B�� | �ڢ� | C�� | �٢ڢ� | D�� | �ڢۢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com