
| A. | 漂白粉、次氯酸溶液和明矾都是混合物 | |
| B. | 不能通过化合反应制得FeCl2和Fe(OH)3 | |
| C. | 铁能在氧气中剧烈燃烧,但不能在水蒸气中燃烧 | |
| D. | 用强光照射装满次氯酸的试管(倒置于水槽中)可收集到两种气体 |
分析 A.漂白粉的主要成分为氯化钙、次氯酸钙,次氯酸溶液为HClO和水的混合物,明矾为十二水硫酸铝钾;
B.Fe与氯化铁反应生成氯化亚铁,氢氧化亚铁、氧气和水化合生成氢氧化铁;
C.Fe与氧气反应生成四氧化三铁,Fe与水蒸气高温下发生氧化还原反应生成四氧化三铁和氢气;
D.HClO光照分解生成氧气.
解答 解:A.漂白粉的主要成分为氯化钙、次氯酸钙,次氯酸溶液为HClO和水的混合物,明矾为十二水硫酸铝钾,则明矾为化合物,故A错误;
B.Fe与氯化铁反应生成氯化亚铁,氢氧化亚铁、氧气和水化合生成氢氧化铁,则能通过化合反应制得FeCl2和Fe(OH)3,故B错误;
C.Fe与氧气反应生成四氧化三铁,Fe与水蒸气高温下发生氧化还原反应生成四氧化三铁和氢气,则铁能在氧气中剧烈燃烧,但不能在水蒸气中燃烧,故C正确;
D.HClO光照分解生成氧气,则用强光照射装满次氯酸的试管(倒置于水槽中)可收集到一种气体,故D错误;
故选C.
点评 本题考查物质的性质,为高频考点,把握物质的性质、发生的反应为解答的关键,注意元素化合物知识的综合应用,题目难度不大.


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:选择题
| A. | $\frac{{{{10}^{-8}}+{{10}^{-10}}}}{2}mol/L$ | B. | $\frac{{{{10}^{-6}}+{{10}^{-4}}}}{2}mol/L$ | ||
| C. | (10-8+10-10)mol/L | D. | 2×10-10mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu(NO3)2溶液可作电解质溶液 | |
| B. | 在电解质溶液中,电子由负极流向正极 | |
| C. | 锌极的质量先减小后增大 | |
| D. | 可用镁作正极材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂水解的产物是高级脂肪酸和丙三醇 | |
| B. | 油脂属于混合物 | |
| C. | 油脂、乙醇是人体必需的营养物质 | |
| D. | 水果因含有酯类物质而具有香味 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
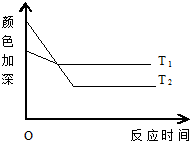 反应A+B?2C,其中A为有色气态物质,其混合物颜色深浅与反应时间、温度(t)之间的关系如图所示(B、C均为无色物质):
反应A+B?2C,其中A为有色气态物质,其混合物颜色深浅与反应时间、温度(t)之间的关系如图所示(B、C均为无色物质):查看答案和解析>>
科目:高中化学 来源: 题型:解答题
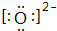 ;
;| 危险性 |  |
| 储运要求 | 远离金属粉末、氨、烃类、醇类物质;设置氯气检测仪 |
| 泄漏处理 | NaOH、NaHSO3溶液吸收 |
| 包装 | 钢瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金 | B. | 硫磺 | C. | 黄铜 | D. | 黄铁矿 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com