
【题目】化学与环境、科学、技术密切相关。下列有关说法中正确的是( )
A.华为首款5G手机搭载了智能的7nm制程SoC麒麟980芯片,此芯片主要成分是二氧化硅
B.用于制作N95型口罩的“熔喷布”主要原料是聚丙烯,聚丙烯的分子长链上无支链
C.国产飞机C919用到的氮化硅陶瓷是传统有机非金属材料
D.侯氏制碱法的工艺过程中应用了物质溶解度的差异
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种重要漂白剂,实验室可按下图装置制取NaClO2晶体。

已知:Ⅰ.A中发生的反应为:2ClO2+H2O2+2NaOH=2NaClO2+O2+2H2O
Ⅱ.NaClO2受热易分解,温度高于60℃时分解成NaClO3和NaCl。
(1)已知ClO2与Cl2类似具有漂白性,请设计检验ClO2漂白性的实验方案______。
(2)A中用冰水浴的目的是______。
(3)装置B的作用是______。
(4)测定样品中NaClO2的质量分数的实验过程如下:
步骤一:称0.5000 g样品,加入适量蒸馏水和过量的KI晶体和硫酸,发生如下反应:ClO![]() +4I﹣+4H+=2H2O+2I2+Cl﹣
+4I﹣+4H+=2H2O+2I2+Cl﹣
步骤二:将所得混合液稀释成100 mL待测溶液。取25.00 mL待测溶液,加入淀粉溶液作指示剂,用0.2000 mol·L-1 Na2S2O3标准液滴定至终点,测得消耗标准溶液体积的平均值为15.00 mL(滴定过程中发生反应:I2+2S2O32-=2I﹣+S4O62-)。
①配制100 mL 0.2000 mol·L-1Na2S2O3标准溶液需要用到的玻璃仪器有烧杯、胶头滴管、______。
②请计算所称取样品中NaClO2的质量分数_______________。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以废旧磷酸亚铁锂正极材料(主要成分为LiFePO4,含炭黑、铝等杂质)为原料可制备LiOH溶液和FePO4。
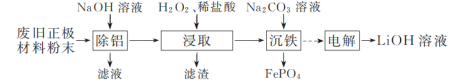
(1)“除铝”时反应的离子方程式为______________________________。
(2)试从沉淀溶解平衡移动的角度解释“浸取时加入H2O2、稀盐酸”可促进LiFePO4溶解的原因:______。
(3)“浸取”所得滤液中,磷元素的存在形式主要是________(填字母)。
a. PO![]() b. H3PO4 c. H2PO
b. H3PO4 c. H2PO![]()
(4)“沉铁”时铁、磷的沉淀率随溶液pH的变化如图1所示。pH>2.5后磷元素的沉淀率逐渐下降,原因是_____________________。
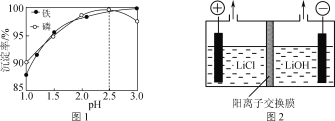
(5)“电解”制备LiOH的原理如图2所示,装置中使用阳离子交换膜将电解槽隔成阳极室和阴极室的目的是________________________________________。
(6)LiOH和(NH4)2Fe(SO4)2、H3PO4反应得到LiFePO4、NH4HSO4。写出该反应的化学方程式:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁-空气电池的总反应方程式为:2Mg+O2+2H2O=2Mg(OH)2,其工作原理如图所示,下列说法不正确是
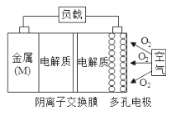
A.该电池的正极反应方程式为O2+4e-+2H2O=4OH-
B.为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜
C.该电池中电子从金属电极流出,流经电解质到多孔电极
D.采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的有几项( )
①热稳定性:Na2CO3>NaHCO3
②常温时在水中的溶解度:NaHCO3<Na2CO3
③Na2CO3不能转化成NaHCO3,而NaHCO3能转化成Na2CO3
④NaHCO3加热至200℃左右,可完全分解,利用这种性质,可由NaHCO3制取纯碱
⑤当NaHCO3与Na2CO3质量相同时,分别跟足量盐酸反应,NaHCO3可得到较多的二氧化碳
⑥Na2CO3·10H2O在空气中会风化
⑦某物质焰色反应呈黄色,该物质一定是钠盐
A.4B.5C.6D.7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】单萜类化合物香叶醇是香精油的主要成分之一。在酸性溶液中,香叶醇可以转化为环状单萜α—松油醇:

![]()
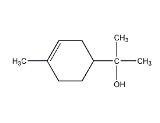
关于香叶醇和α—松油醇,下列说法正确的是( )
A.香叶醇能在铜丝催化下和氧气氧化生成醛,但α—松油醇不能
B.两者互为同分异构体,分子式是C10H20O
C.两者分子中所有原子均处于同一平面
D.两者均能使溴的四氯化碳溶液褪色,是发生消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上采用的一种污水处理方法如下:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3。Fe(OH)3具有吸附性,可吸附污物而沉积下来,有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用该原理处理污水,设计装置如图所示。下列说法正确的是
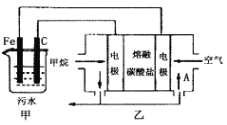
A.为了增加污水的导电能力,应向污水中加入适量的H2SO4溶液
B.甲装置中Fe电极的反应为Fe-3e-=Fe3+
C.当乙装置中有1.6gCH4参加反应,则C电极理论上生成气体体积为4.48L
D.为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时,循环的物质A为CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机合成在化工医药领域应用广泛,下图是一种新型药物合成路线。
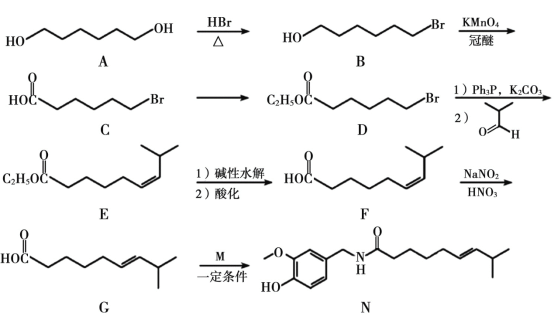
回答下列问题:
(1)A 的系统命名法(CCS)名称为________,D 中官能团的名称为________。
(2)B→C 的反应类型为________,从反应所得液态有机混合物中提纯 B 的常用方法为________。
(3)C→D 的化学方程式为________。C 和 D 在下列哪种检测仪上显示出的信号峰是完全相同的_________
A.元素分析仪 b.红外光谱仪 c.核磁共振仪 d.质谱仪
(4)C 的同分异构体 W(不考虑手性异构)可发生银镜反应,且 1 mol W 最多与 2 molNaOH 发生反应,产物之一可被氧化成二元醛,满足上述条件的 W 有________种。若 W 的核磁共振氢谱具有四组峰,则其结构简式为________。
(5)F 与 G 的关系为(填序号)________。
A.碳链异构 b.官能团类别异构 c.顺反异构 d.官能团位置异构
(6)M 的结构简式为________。
(7)参照上述合成路线,以![]() 和
和![]() 为原料制备医药中间体
为原料制备医药中间体![]() ,写出合成路线流程图_________________________________________________________________。
,写出合成路线流程图_________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CxHy+H2O→CO+CO2+H2(未配平),工业上用甲烷、乙烷的混合气体利用上述反应生成氢气,反应后气体经干燥组成如下表所示,计算原混合气体中甲烷与乙烷的物质的量之比____________。
组分 | CO | CO2 | H2 |
体积分数 | 20% | 5% | 75% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com