
 ;
;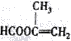 ;
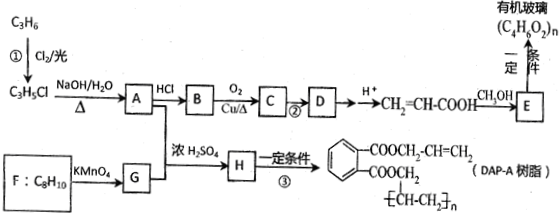
;分析 丙烯系列转化得到CH2=CHCOOH,由转化关系可知,CH2=CHCH3与氯气发生取代反应生成CH2=CHCH2Cl,CH2=CHCH2Cl在碱性条件下水解得A为CH2=CHCH2OH,A与HCl加成可得B为CH2ClCH2CH2OH或CH3CHClCH2OH,B中的醇羟基被氧化成羧基,C→D是在氢氧化钠的醇溶液发生消去反应,所以C为CH2ClCH2COOH或CH3CHClCOOH,D为CH2=CHCOONa,D酸化得到CH2=CHCOOH,CH2=CHCOOH与CH3OH反应生成E为CH2=CHCOOCH3,发生加聚反应得有机玻璃为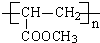 ,由
,由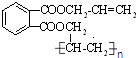 可推知H为
可推知H为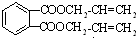 ,所以G为
,所以G为 ,则F为
,则F为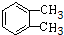 .
.
解答 解:丙烯系列转化得到CH2=CHCOOH,由转化关系可知,CH2=CHCH3与氯气发生取代反应生成CH2=CHCH2Cl,CH2=CHCH2Cl在碱性条件下水解得A为CH2=CHCH2OH,A与HCl加成可得B为CH2ClCH2CH2OH或CH3CHClCH2OH,B中的醇羟基被氧化成羧基,C→D是在氢氧化钠的醇溶液发生消去反应,所以C为CH2ClCH2COOH或CH3CHClCOOH,D为CH2=CHCOONa,D酸化得到CH2=CHCOOH,CH2=CHCOOH与CH3OH反应生成E为CH2=CHCOOCH3,发生加聚反应得有机玻璃为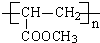 ,由
,由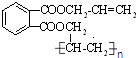 可推知H为
可推知H为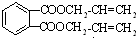 ,所以G为
,所以G为 ,则F为
,则F为 .
.
(1)由上面的分析可知,B为CH2ClCH2CH2OH或CH3CHClCH2OH,
故答案为:CH2ClCH2CH2OH或CH3CHClCH2OH;
(2)E为CH2=CHCOOCH3,名称为丙烯酸甲酯,
故答案为:丙烯酸甲酯;
(3)A+G→H的化学方程式是: ,
,
故答案为: ;
;
(4)W是E(CH2=CHCOOCH3)的同分异构体,具有下列结构特征:①核磁共振氢谱有3个吸收峰,且峰面积之比为1:2:3;②既能发生银镜反应,又能与NaOH溶液反应,含有甲酸形成的酯基,W的结构简式是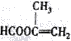 ,
,
故答案为: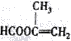 ;
;
(5)a.C→D发生消去反应,的反应条件是NaOH醇溶液、加热,故a错误;
b.B为CH2ClCH2CH2OH或CH3CHClCH2OH,含有醇羟基、氯原子,可以发生消去反应、取代反应、氧化反应,故b正确;
c.1molDAP-A树脂含有 2n mol酯基(羧酸与醇形成的酯基),最多能消耗2n molNaOH,故c正确;
d.D为CH2=CHCOONa,属于强碱弱酸盐,常温下D的水溶液显碱性,促进了水的电离,故d错误.
故选:bc.
点评 本题考查有机物的推断与合成,充分利用有机物的结构与反应条件进行分析,需要学生熟练掌握官能团的性质与转化,较好地考查学生分析推理能力,是对有机化学基础的综合考查.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 往溶液中加入适量的氢氧化钠,使溶液中c(Na+)=c(CH3 COO-) | |
| B. | 将溶液与10 mLpH=10的NaOH溶液混合 | |
| C. | 将溶液与10 mL浓度为a mol•L-1的NaOH溶液混合 | |
| D. | 将溶液稀释到10 L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过滤操作时,为了过滤效果好,要用玻璃棒搅拌 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 蒸发操作时,为了防止局部过热,要用玻璃棒搅拌 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com