
【题目】A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同周期,C、D、E同处另一周期,C、A可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙,B是最活泼的非金属元素,D是地壳中含量最高的金属元素,E的最高价氧化物对应的水化物是周期表中最强的含氧酸。
(1)元素B在周期表中的位置是_________,甲的电子式是_______。
(2)单质D与C的最高价氧化物对应水化物的水溶液反应的离子方程式是___________。
(3)单质E与C的最高价氧化物对应水化物的水溶液反应的化学方程式是________。
(4)物质乙与水反应的化学方程式____________。
【答案】第2周期VII A族 ![]() 2Al + 2OH- + 2H2O = 2AlO2- + 3H2 ↑ Cl2 + 2NaOH =NaCl + NaClO + H2O 2Na2O2 + 2H2O = 4NaOH + O2↑
2Al + 2OH- + 2H2O = 2AlO2- + 3H2 ↑ Cl2 + 2NaOH =NaCl + NaClO + H2O 2Na2O2 + 2H2O = 4NaOH + O2↑
【解析】
A、B、C、D、E都是短周期元素,原子序数依次增大,C、A可按原子个数比2:l和1:1分别形成两种离子化合物甲和乙,则甲为Na2O、乙为Na2O2,A是O元素,C是Na元素,B是最活泼的非金属元素,则B是F元素,D是地壳中含量最高的金属元素,则D是Al元素,E的最高价氧化物对应的水化物是最强的含氧酸,则E是Cl元素。
(1)B为氟元素,位于周期表中第二周期ⅦA族,甲为Na2O,电子式为![]() ,故答案为:第二周期ⅦA族;
,故答案为:第二周期ⅦA族;![]() ;
;
(2)铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,离子反应方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(3)氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠与水,反应方程式为:Cl2+2NaOH═NaCl+NaClO+H2O,故答案为:Cl2+2NaOH═NaCl+NaClO+H2O;
(4)过氧化钠与水反应生成氢氧化钠与氢气,反应方程式为:2Na2O2+2H2O═4NaOH+O2↑,故答案为:2Na2O2+2H2O═4NaOH+O2↑。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】(1)元素周期表是我们研究物质性质、结构的重要工具,对周期表的熟悉和掌握程度直接影响我们对化学的学习。元素周期表共有七个周期十六个族;第ⅠA族元素(除氢外)的最高价氧化物对应水化物都是易溶于水的强碱,又称为___元素,卤族元素位于第__纵行,最高正价与最低负价的绝对值相等的元素位于___族。
(2)A、B、C、D、E、F、G为原子序数依次增大的前20号元素(此时不考虑稀有气体元素),在周期表中B和C,C和E分别相邻,B、E、G的最外层电子数之和为12。已知部分元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
A | 该元素有一种核素质量数为1 |
B | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
D | 原子的次外层电子数是最外层电子数的两倍 |
①由元素A、B形成的核外电子总数为10e-的两种微粒:___,___(写化学式)。
②C元素在周期中的位置:___。
③C、D形成的化合物在通讯上的重要用途___。
④E与G两元素可形成化合物,用电子式表示其化合物的形成过程:___。
⑤用化学方程式表示B、D两种元素的非金属性强弱___。
⑥A、B、F三种元素形成的一种常见化合物易溶于水,受热易分解,可用于制作干电池,该物质的电子式是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据下图装置,下列叙述不正确的是
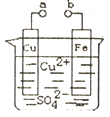
A. a和b不连接时,铁片上会有金属铜析出
B. a和b用导线连接时,铜片上发生的反应为:Cu2++2e-=Cu
C. a和b分别连接直流电源正、负极,Cu2+向铜电极移动
D. 无论a和b是否连接,铁片均会溶解,溶液颜色都会发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向湿法炼锌的电解液中同时加入Cu和CuSO4,可生成CuCl沉淀除去Cl-,降低对电解的影响,反应原理如下:Cu(s)+Cu2+(aq)![]() 2Cu+(aq) ΔH1=akJ/mol;Cl-(aq)+Cu+(aq)
2Cu+(aq) ΔH1=akJ/mol;Cl-(aq)+Cu+(aq)![]() CuCl(s) ΔH2=bkJ/mol,实验测得电解液pH对溶液中残留c(Cl-)的影响如图所示。下列说法正确的是( )
CuCl(s) ΔH2=bkJ/mol,实验测得电解液pH对溶液中残留c(Cl-)的影响如图所示。下列说法正确的是( )
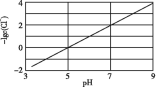
A. 溶液pH越大,Ksp(CuCl)增大
B. 向电解液中加入稀硫酸,有利于Cl-的去除
C. 反应达到平衡后,增大c(Cu2+),c(Cl-)减小
D. ![]() Cu(s)+
Cu(s)+![]() Cu2+(aq)+Cl-(aq)
Cu2+(aq)+Cl-(aq)![]() CuCl(s)的ΔH=(a+2b)kJ/mol
CuCl(s)的ΔH=(a+2b)kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,可逆反应A(g)+3B(g)![]() 2C(g)达到平衡的标志是( )
2C(g)达到平衡的标志是( )
A. C生成的速率是A反应速率的2倍
B. A、B、C的浓度不再变化
C. 单位时间内生成nmol A,同时生成3nmol B
D. A、B、C的分子数之比为1∶3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述中正确的是( )
A. 0.3 mol Cu与足量稀硝酸充分反应,可收集到4.48L气体
B. 由NO2和N2O4组成的混合物46g中共含有2NA个N原子
C. 常温常压下,16g甲烷分子中所含质子数为10NA
D. 0.2mol/L的NH4NO3溶液中所含N原子的数目为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源、信息、材料是新科技革命的三大支柱,现有一种叫HEMA的材料,是用来制备软质隐形眼镜的,其结构简式如图,则合成它的单体为( )
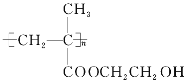
A. CH3—CH=CH—COOH CH3CH2OH
B. 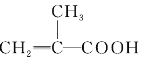 HOCH2CH2OH
HOCH2CH2OH
C. CH2=CH—CH2COOH HOCH2CH2OH
D. 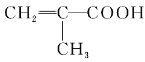 CH3CH2OH
CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无色的混合气体甲,可能含NO、CO2、NO2、NH3、N2中的几种,将100mL甲气体依次通过下图实验的处理,结果得到酸性溶液,几乎无气体剩余,则甲气体的组成为
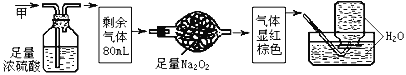
A.NH3、NO2、N2B.NH3、NO、CO2
C.NH3、NO2、CO2D.NO、CO2、N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容密闭容器中,当物质的下列物理量不再变化时,不能表明反应:A(s)+2B(g)![]() C(g)+D(g)已达平衡的是( )
C(g)+D(g)已达平衡的是( )
A.混合气体的压强B.混合气体的密度
C.B的物质的量浓度D.混合气体的平均相对分子质量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com