
| 选项 | A | B | C | D |
| 图标 | 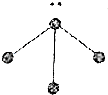 | 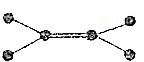 | 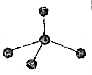 |  |
| 化学式 | NH3 | C2H4 | CCl4 | CO2 |
| A. | A | B. | B | C. | C | D. | D |
 教学练新同步练习系列答案
教学练新同步练习系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醋酸除去水垢:2H++CaCO3═Ca2++CO2↑+H2O | |
| B. | MnO2 与浓盐酸反应制Cl2:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2Cl-+Cl2↑+2H2O | |
| C. | Na与水产生H2:Na+H2O═Na++OH-+H2↑ | |
| D. | Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
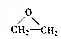 称为环氧乙烷,它在一定条件下,能与氢氧化物发生加成反应,氢原子加到氧原子上,其他部分加在碳原子上,下列对环氧乙烷的衍生物
称为环氧乙烷,它在一定条件下,能与氢氧化物发生加成反应,氢原子加到氧原子上,其他部分加在碳原子上,下列对环氧乙烷的衍生物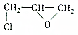 的叙述正确的是( )
的叙述正确的是( )| A. | 能与水反应生成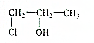 | |
| B. | 能碱性水解生成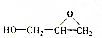 | |
| C. | 在一定条件下可以合成甘油 | |
| D. | 加入AgNO3溶液能生成难溶于硝酸的白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制取乙烯:乙醇与浓硫酸共热至140℃ | |
| B. | 除去甲烷中的乙炔:混合气体通过酸性高锰酸钾溶液,再经浓硫酸干燥 | |
| C. | 除去苯中的苯酚:加入NaOH溶液振荡,静置分层后,除去水层 | |
| D. | 检验氯乙烷中的氯元素:氯乙烷与NaOH的水溶液共热后,加入AgNO3溶液有白色沉淀生成证明含CI- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na[Au(CN)2]可溶于水 | |
| B. | 化合物Na[Au(CN)2]中金元素的化合价为+2 | |
| C. | 金化学性质稳定,不与任何物质反应 | |
| D. | 在提炼过程中含金元素的物质始终作氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸能够使紫色石蕊试剂变红,所以乙酸是强酸 | |
| B. | 食醋除去水垢的现象证明了酸性:乙酸>碳酸 | |
| C. | 乙酸与乙醇发生的酯化反应不属于取代反应 | |
| D. | 在制备乙酸乙酯的实验中,用18O标记乙醇,在产物乙酸乙酯中检测不到18O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 温度/℃ | 500 | 525 | 550 | 575 | 600 |
| 平衡转化率/% | 93.5 | 90.5 | 85.6 | 80.0 | 73.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实 验 内 容 | 实 验 试 剂 | 实 验 现 象 |
| 探究氧化性 | 取适量碘化钾淀粉溶液于试管中,加入过氧化氢溶液 | 溶液变蓝色 |
| 探究不稳定性 | 取适量过氧化氢溶液于试管中,加热, 用带火星的木条检验 | 产生气泡,木条复燃 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com