
| 0.318g |
| 0.4g |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、①④⑤ | B、①③④ |
| C、①③④⑤ | D、①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
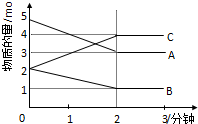 某可逆反应在某体积为5L的密闭容器中进行,在从0-3分钟各物质的量的变化情况如图所示(A、B、C均为气体).
某可逆反应在某体积为5L的密闭容器中进行,在从0-3分钟各物质的量的变化情况如图所示(A、B、C均为气体).查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图表示A~E五种物质间的相互转化关系,其中A为淡黄色固体,B为单质.试回答下列问题:
如图表示A~E五种物质间的相互转化关系,其中A为淡黄色固体,B为单质.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
 现有一定量含有氧化钠杂质的过氧化钠样品,用如图的实验装置测定过氧化钠样品的纯度.试回答下列问题:
现有一定量含有氧化钠杂质的过氧化钠样品,用如图的实验装置测定过氧化钠样品的纯度.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在标况下,11.2 L NO与11.2 L O2混合后所含分子数为0.75 NA |
| B、常温常压下,16gO3所含的电子数8NA |
| C、0.1 mol Na2O2晶体中含有0.4 NA个离子 |
| D、铝跟氢氧化钠溶液反应生成1 mol氢气时,转移的电子数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com