
氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
已知:CH4(g)+H2O(g)===CO(g)+3H2(g)
ΔH=206.2 kJ·mol-1
CH4(g)+CO2(g)===2CO(g)+2H2(g)
ΔH=247.4 kJ·mol-1
2H2S(g)===2H2(g)+S2(g)
ΔH=169.8 kJ·mol-1
(1)以甲烷为原料制取氢气是工业上常用的制氢方法。
CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为________________________________________________________________________。
(2)H2S热分解制氢时,常向反应器中通入一定比例空气,使部分H2S燃烧,其目的是____________________________;燃烧生成的SO2与H2S进一步反应,生成物在常温下均非气体,写出该反应的化学方程式:_____________________________________________。
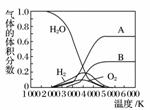
(3)H2O的热分解也可得到H2,高温下水分解体系中主要气体的体积分数与温度的关系如下图所示。图中A、B表示的物质依次是________________________。
(5)Mg2Cu是一种储氢合金。350 ℃时,Mg2Cu与H2反应,生成MgCu2和仅含一种金属元素的氢化物(其中氢的质量分数为0.077)。Mg2Cu与H2反应的化学方程式为________________________________________________________________________。
科目:高中化学 来源: 题型:
工业上用电解法处理含镍酸性废水并得到单质Ni的原理如图所示。
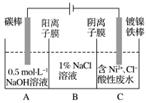
下列说法不正确的是( )
已知:①Ni2+在弱酸性溶液中发生水解
②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)
A.碳棒上发生的电极反应:4OH--4e-===O2↑+2H2O
B.电解过程中,B中NaCl溶液的物质的量浓度将不断减少
C.为了提高Ni的产率,电解过程中需要控制废水pH
D.若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
已知1 g氢气完全燃烧生成液态水时放出热量143 kJ,18 g水蒸气变成液态水放出44 kJ的热量。其他相关数据如下表:
| O===O(g) | H—H | H—O | |
| 1 mol化学键断裂时需要吸收的能量/kJ | 496 | x | 463 |
则表中x为( )
A.920 B.557
C.436 D.188
查看答案和解析>>
科目:高中化学 来源: 题型:
同一反应,反应物状态不同时
S(g)+O2(g)===SO2(g) ΔH1<0
S(s)+O2(g)===SO2(g) ΔH2<0
则ΔH1____ΔH2。
查看答案和解析>>
科目:高中化学 来源: 题型:
能源分类相关图如下图所示,下列四组选项中,全部符合图中阴影部分的能源是( )
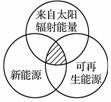
A.煤炭、石油、沼气
B.水能、生物能、天然气
C.太阳能、风能、潮汐能
D.地热能、海洋能、核能
查看答案和解析>>
科目:高中化学 来源: 题型:
某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变为H2、CO。其过程如下:
mCeO2 (m-x)CeO2·xCe+xO2
(m-x)CeO2·xCe+xO2
(m-x)CeO2·xCe+xH2O+xCO2 mCeO2+xH2+xCO
mCeO2+xH2+xCO
下列说法不正确的是( )
A.该过程中CeO2没有消耗
B.该过程实现了太阳能向化学能的转化

C.右图中ΔH1=ΔH2+ΔH3
D.以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH--2e-===CO +2H2O
+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列推论正确的是( )
A.S(g)+O2(g)===SO2(g) ΔH1;S(s)+O2===SO2(g) ΔH2,则ΔH1>ΔH2
B.C(石墨,s)===C(金刚石,s) ΔH=+1.9 kJ·mol-1,则由石墨制取金刚石的反应是吸热反应,金刚石比石墨稳定
C.NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l) ΔH=-57.4 kJ·mol-1,则:含20 g NaOH的稀溶液与稀盐酸完全反应,放出的热量为28.7 kJ
D.2C(s)+O2(g)===2CO(g) ΔH=-221 kJ·mol-1,则碳的燃烧热等于110.5 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
根据前四周期元素原子核外电子排布特点,回答下列问题:
(1)外围电子层有2个未成对电子的有________;有3个未成对电子的有________。
(2)未成对电子数与周期数相等的元素有________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com