(2012?朝阳区一模)高铁酸钠(Na
2FeO
4)具有很强的氧化性,是一种新型的绿色净水消毒剂.工业上可以通过次氯酸钠氧化法制备高铁酸钠,生产过程如下:
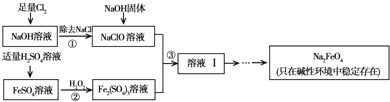
回答下列问题:
(1)氢氧化钠的电子式是
.
(2)经过步骤①后,加入NaOH固体的原因是
Na2FeO4只在碱性环境中稳定存在,所以加入氢氧化钠可以调节溶液显碱性
Na2FeO4只在碱性环境中稳定存在,所以加入氢氧化钠可以调节溶液显碱性
.
(3)步骤②反应的离子方程式是
2Fe2++H2O2+2H+=2Fe3++2H2O
2Fe2++H2O2+2H+=2Fe3++2H2O
.
(4)从溶液Ⅰ中分离出Na
2FeO
4后,还有副产品Na
2SO
4、NaCl,则步骤③中反应的离子方程式为
2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O
2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O
.
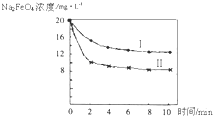
(5)将一定量的Na
2FeO
4投入到pH不同的污水中(污水中其余成分均相同),溶液中Na
2FeO
4浓度变化如图曲线Ⅰ、Ⅱ所示,试推测曲线I比曲线II对应的污水pH
高
高
(填“高”或“低”).
(6)通过计算得知Na
2FeO
4的消毒效率(以单位质量得到的电子数表示)比氯气的
低
低
(填“高”或“低”),用高铁酸钠代替氯气作净水消毒剂的优点是
既能消毒杀菌又能净水
既能消毒杀菌又能净水
(答出两点即可).



 特高级教师点拨系列答案
特高级教师点拨系列答案 (2012?朝阳区一模)高铁酸钠(Na2FeO4)具有很强的氧化性,是一种新型的绿色净水消毒剂.工业上可以通过次氯酸钠氧化法制备高铁酸钠,生产过程如下:
(2012?朝阳区一模)高铁酸钠(Na2FeO4)具有很强的氧化性,是一种新型的绿色净水消毒剂.工业上可以通过次氯酸钠氧化法制备高铁酸钠,生产过程如下:

