

·ÖĪö £Ø1£©Ļ“µÓŗóŠčŅŖøÉŌļ£¬æŲÖĘĪĀ¶Č±ÜĆāŹ§Č„½į¾§Ė®£»
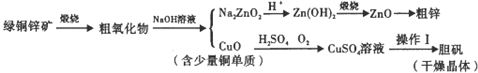
£Ø2£©“ÖŃõ»ÆĪļĪŖZnO£¬ÓėŃõ»ÆĀĮŠŌÖŹĻąĖĘ£¬ZnOÓėĒāŃõ»ÆÄĘ·“Ӧɜ³ÉNa2ZnO2ÓėĖ®£»
£Ø3£©ĖįŠŌĢõ¼žĻĀ£¬Ź¹Cu×Ŗ»ÆĪŖĮņĖįĶ£»
£Ø4£©æÉŅŌ·ĄÖ¹µ¹Īü£¬ĶØČėŃõĘų£¬¶žŃõ»ÆµŖ”¢NOÄܱ»ĒāŃõ»ÆÄĘČÜŅŗĶźČ«ĪüŹÕ£»
£Ø5£©¢Ł¼ÓĖ®Ź¹ĮæĘų×°ÖĆ×óÓŅĮ½¹ÜŠĪ³ÉŅŗĆęøß¶Č²ī£¬ŅŗĆęøß¶Č²ī±£³Ö²»±ä£¬ĖµĆ÷ĘųĆÜŠŌĮ¼ŗĆ£»
¢ŚČōµ¼Ęų¹ÜÓė·ÖŅŗĀ©¶·ÉĻæŚ²»ĻąĮ¬£¬ŅņµĪČėĮņĖįÅųöµÄæÕĘų»įµ±³ÉĒāĘųĢå»ż£»
¢ŪČōĀĢĶŠææóŹÆĪŖ550g£¬ŌņÉś³É×īÖÕÖʵƓ֊æ113.4g£¬øł¾ŻÉś³ÉĒāĘųĢå»ż¼ĘĖć7g“ÖŠæÖŠZnµÄÖŹĮ棬½ų¶ų¼ĘĖć113.4g“ÖŠæÖŠZnµÄÖŹĮ棬øł¾ŻZnŌŖĖŲŹŲŗćæÉµĆ¹ŲĻµŹ½£ŗZn£ØOH£©2”«Zn£¬½«ĆæŅ»²½µÄĖšŹ§ĀŹ”¢ĄūÓĆĀŹ¶¼×Ŗ»ÆĪŖZn£ØOH£©2ĄūÓĆĀŹ£¬ÉčZn£ØOH£©2ÖŹĮæ·ÖŹżĪŖy£¬±ķŹ¾³öĄūÓƵÄZn£ØOH£©2µÄÖŹĮ棬½įŗĻ¹ŲĻµŹ½¼ĘĖć£®
½ā“š ½ā£ŗ£Ø1£©Ļ“µÓŗóŠčŅŖøÉŌļ£¬µØ·ÆÖŠ½į¾§Ė®ČŻŅ׏§Č„£¬Ó¦µĶĪĀŗęøÉ£¬
¹Ź“š°øĪŖ£ŗµĶĪĀŗęøÉ£»
£Ø2£©“ÖŃõ»ÆĪļĪŖZnO£¬ÓėŃõ»ÆĀĮŠŌÖŹĻąĖĘ£¬ZnOÓėĒāŃõ»ÆÄĘ·“Ӧɜ³ÉNa2ZnO2ÓėĖ®£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗZnO+2NaOH=Na2ZnO2+H2O£¬
¹Ź“š°øĪŖ£ŗZnO+2NaOH=Na2ZnO2+H2O£»
£Ø3£©CuOÖŠŗ¬ÓŠÉŁĮæµÄCu£¬CuÓėĮņĖį²»·“Ó¦£¬µ«ĶØČėŃõĘų£¬æÉŅŌŹ¹Cu×Ŗ»ÆĪŖĮņĖįĶ£¬
¹Ź“š°øĪŖ£ŗŹ¹Cu×Ŗ»ÆĪŖĮņĖįĶ£»
£Ø4£©Ö±½ÓÓĆĒāŃõ»ÆÄĘČÜŅŗĪüŹÕĪ²Ęų£¬æÉÄÜ·¢Éśµ¹ĪüĪ£ĻÕ£¬²¢ĒŅNOµ„¶Ą²»Äܱ»ĒāŃõ»ÆÄĘČÜŅŗĪüŹÕ£¬ČōÓĆĶ¼2×°ÖĆĮ¬ŌŚĶ¼1µÄA”¢BÖ®¼ä£¬æÉŅŌ·ĄÖ¹µ¹Īü£¬ÓÉÓŚĶØČėŃõĘų£¬¶žŃõ»ÆµŖ”¢NOÄܱ»ĒāŃõ»ÆÄĘČÜŅŗĶźČ«ĪüŹÕ£¬
¹Ź“š°øĪŖ£ŗ·ĄÖ¹µ¹Īü£»¶žŃõ»ÆµŖ”¢NOÄܱ»ĒāŃõ»ÆÄĘČÜŅŗĶźČ«ĪüŹÕ£»
£Ø5£©¢Ł¼ģŃé×°ÖĆĘųĆÜŠŌ·½·Ø£ŗĻņĮæĘų¹ÜÓŅ¶Ė¼ÓĖ®ÖĮÓŅ¶ĖŅŗĆęøßÓŚ×ó¶ĖŅŗĆę£¬ČōŅŗĆęøß¶Č²»·¢Éś±ä»Æ£¬ŌņĘųĆÜŠŌĮ¼ŗĆ£¬
¹Ź“š°øĪŖ£ŗĻņĮæĘų¹ÜÓŅ¶Ė¼ÓĖ®ÖĮÓŅ¶ĖŅŗĆęøßÓŚ×ó¶ĖŅŗĆę£¬ČōŅŗĆęøß¶Č²»·¢Éś±ä»Æ£¬ŌņĘųĆÜŠŌĮ¼ŗĆ£»
¢ŚČōµ¼Ęų¹ÜÓė·ÖŅŗĀ©¶·ÉĻæŚ²»ĻąĮ¬£¬ŅņµĪČėĮņĖįÅųöµÄæÕĘų»įµ±³ÉĒāĘųĢå»ż£¬µ¼ÖĀ²ā¶ØĒāĘųĢå»żĘ«“󣬲ā¶ØZnµÄ“æ¶ČĘ«“󣬵¼Ęų¹ÜÓė·ÖŅŗĀ©¶·ÉĻæŚĻąĮ¬£¬æÉŅŌĻū³żĻ”ĮņĖįµĪČėÅųöµÄæÕĘų¶ŌĒāĘųĢå»żµÄÓ°Ļģ£¬
¹Ź“š°øĪŖ£ŗæÉŅŌĻū³żĻ”ĮņĖįµĪČėÅųöµÄæÕĘų¶ŌĒāĘųĢå»żµÄÓ°Ļģ£»
¢ŪČōĀĢĶŠææóŹÆĪŖ550g£¬ŌņÉś³É×īÖÕÖʵƓ֊æ113.4g£¬
7g“ÖŠæÖŠZn·“Ó¦ĒāĘųĪŖ$\frac{2.24L}{22.4L/mol}$=0.1mol£¬Óɵē×Ó×ŖŅĘŹŲŗć£¬Ōņ7g“ÖŠæÖŠZnĪŖ$\frac{0.1mol”Į2}{2}$=0.1mol£¬ÖŹĮæĪŖ0.1mol”Į65g/mol=6.5g£¬113.4g“ÖŠæÖŠZnµÄÖŹĮæĪŖ6.5g”Į$\frac{113.4g}{7g}$=105.3g£¬
Éč550gĀĢĶŠææóŹÆÖŠZn£ØOH£©2µÄÖŹĮæ·ÖŹżĪŖy£¬Ōņ£ŗ
Zn£ØOH£©2”«”«”«”«”«”«”«”«Zn
99 65
550g”Įy”Į£Ø1-10%£©”Į90% 105.3g
ĖłŅŌ£ŗ99£ŗ65=550g”Įy”Į£Ø1-10%£©”Į90%£ŗ105.3g
½āµĆy=36%£¬
¹Ź“š°øĪŖ£ŗ36%£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹÖʱøŹµŃ飬Éę¼°ĪļÖŹµÄ·ÖĄėĢį“攢¶Ō×°ÖƵķÖĪöĘĄ¼Ū”¢»ł±¾²Ł×÷”¢ĪļÖŹŗ¬Įæ²ā¶ØµČ£¬ŹĒ¶Ōѧɜ×ŪŗĻÄÜĮ¦µÄ漲飬£Ø5£©ÖŠ¼ĘĖćĪŖŅדķµć”¢ÄŃµć£¬ÄѶČÖŠµČ£®


 ø÷µŲĘŚÄ©ø“Ļ°ĢŲѵ¾ķĻµĮŠ“š°ø
ø÷µŲĘŚÄ©ø“Ļ°ĢŲѵ¾ķĻµĮŠ“š°ø Š”²©ŹæĘŚÄ©“³¹Ų100·ÖĻµĮŠ“š°ø
Š”²©ŹæĘŚÄ©“³¹Ų100·ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
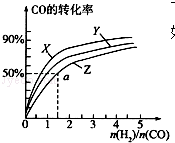 ¼×“¼ŹĒÖŲŅŖµÄČ¼ĮĻ£¬ÓŠ¹ćĄ«µÄÓ¦ÓĆĒ°¾°£ŗ¹¤ŅµÉĻŅ»°ćŅŌCOŗĶĪŖŌĮĻŗĻ³É¼×“¼£¬øĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗCO£Øg£©+2H2£Øg£©ØTCH3OH£Øg£©”÷H1=-116kJ•mol-1
¼×“¼ŹĒÖŲŅŖµÄČ¼ĮĻ£¬ÓŠ¹ćĄ«µÄÓ¦ÓĆĒ°¾°£ŗ¹¤ŅµÉĻŅ»°ćŅŌCOŗĶĪŖŌĮĻŗĻ³É¼×“¼£¬øĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗCO£Øg£©+2H2£Øg£©ØTCH3OH£Øg£©”÷H1=-116kJ•mol-1²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ¢ń | ¢ņ |
| A | Ba£ØOH£©2ČÜŅŗÓė¹żĮæNaHCO3ČÜŅŗ»ģŗĻ | NaOHČÜŅŗÓė¹żĮæNaHCO3ČÜŅŗ»ģŗĻ |
| B | ÉŁĮæSO2ĶØČėBa£ØOH£©2ČÜŅŗÖŠ | ¹żĮæSO2ĶØČėBa£ØOH£©2ČÜŅŗÖŠ |
| C | BaCl2ČÜŅŗÓėNa2SO3ČÜŅŗ»ģŗĻ | Ba£ØOH£©2ČÜŅŗÓėH2SO3ČÜŅŗ»ģŗĻ |
| D | ÉŁĮæNaHCO3ČÜŅŗµĪČė³ĪĒåŹÆ»ŅĖ®ÖŠ | ÉŁĮæNaOHČÜŅŗµĪČėCa£ØHCO3£©2ČÜŅŗÖŠ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
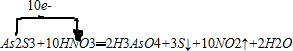 £»
£»²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³ĪĒåĶøĆ÷µÄĪŽÉ«ČÜŅŗ£ŗMnO4- Na+ I- Mg2+ | |
| B£® | ŗ¬ÓŠ0.1mol/L Fe3+ µÄČÜŅŗÖŠ£ŗNa+ Ca2+ SCN- SO42- | |
| C£® | ÓėĀĮʬ·“Ó¦²śÉśĒāĘųµÄČÜŅŗ£ŗCO32- SO42- Na+ NH4+ | |
| D£® | Ź¹·ÓĢŖČÜŅŗ±äŗģµÄČÜŅŗ£ŗNa+ Cl- NO3- Ba2+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 Ņ»ÖÖ¹ā»Æѧµē³ŲµÄ½į¹¹ČēĶ¼£¬µ±¹āÕÕŌŚ±ķĆęĶæÓŠĀČ»ÆŅųµÄŅųʬÉĻŹ±£¬AgCl£Øs£©=AgCl£Øs£©=Ag £Øs£©+Cl£ØAgCl£©£¬[Cl£ØAgCl£©±ķŹ¾Éś³ÉµÄĀČŌ×ÓĪüø½ŌŚĀČ»ÆŅų±ķĆę]£¬½Ó×ÅCl£ØAgCl£©+e-”śCl-£Øaq£©£¬Čō½«¹āŌ“ŅĘ³ż£¬µē³Ų»įĮ¢¼“»Ųø“ÖĮ³õŹ¼×“Ģ¬£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
Ņ»ÖÖ¹ā»Æѧµē³ŲµÄ½į¹¹ČēĶ¼£¬µ±¹āÕÕŌŚ±ķĆęĶæÓŠĀČ»ÆŅųµÄŅųʬÉĻŹ±£¬AgCl£Øs£©=AgCl£Øs£©=Ag £Øs£©+Cl£ØAgCl£©£¬[Cl£ØAgCl£©±ķŹ¾Éś³ÉµÄĀČŌ×ÓĪüø½ŌŚĀČ»ÆŅų±ķĆę]£¬½Ó×ÅCl£ØAgCl£©+e-”śCl-£Øaq£©£¬Čō½«¹āŌ“ŅĘ³ż£¬µē³Ų»įĮ¢¼“»Ųø“ÖĮ³õŹ¼×“Ģ¬£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | ¹āÕÕŹ±£¬µēĮ÷ÓÉYĮ÷ĻņX | |
| B£® | ¹āÕÕŹ±£¬Ptµē¼«·¢ÉśµÄ·“Ó¦ĪŖ2Cl-+2e-ØTCl2 | |
| C£® | ¹āÕÕŹ±£¬Cl-ĻņAgµē¼«ŅĘ¶Æ | |
| D£® | ¹āÕÕŹ±£¬µē³Ų×Ü·“Ó¦ĪŖ£ŗAgCl£Øs£©+Cu+£Øaq£©$\frac{\underline{\;¹ā\;}}{\;}$Ag £Øs£©+Cu2+£Øaq£©+Cl-£Øaq£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com