
【题目】实验室用下述装置制取氯气,并用氯气进行下列实验.看图1回答下列问题:
(1)A、B两仪器的名称:A , B .
(2)洗气装置C是为了除去Cl2中的HCl气体,D是为了干燥Cl2 , 则C、D中应分别放入下列溶液中的C;D . ①NaOH溶液②饱和食盐水③AgNO3溶液 ④浓H2SO4
(3)E中为红色干布条,F中为红色湿布条,可观察到的现象是 .
(4)G是浸有淀粉KI溶液的棉花球,G处现象是棉花球表面变成 . 反应的离子方程式是 , H是浸有NaBr溶液的棉花球,H处现象是棉花球表面变成 .
(5)P处为尾气吸收装置,可选用图2装置中的 .
【答案】
(1)分液漏斗;圆底烧瓶
(2)②;④
(3)E中无变化,F中红色布条褪色
(4)蓝色;2I﹣+Cl2═2Cl﹣+I2;橙色
(5)B
【解析】解:(1)装置图中仪器作用和图形可知是利用分液漏斗向烧瓶中加入浓盐酸加热反应生成氯气的发生装置;故答案为:分液漏斗;圆底烧瓶;(2)洗气装置C是为了除去Cl2中的HCl气体,选择饱和食盐水吸收氯化氢,D是为了干燥Cl2 , 选择浓硫酸干燥氯气;故答案为:②④;(3)氯气能使湿润的有色布条褪色,不能使干燥的有色布条褪色,所以E中无变化,F中红色布条褪色;故答案为:E中无变化,F中红色布条褪色;(4)通入Cl2时发生反应2I﹣+Cl2═2Cl﹣+I2 , 生成的I2遇淀粉溶液变蓝色.Cl2也能将Br﹣氧化为Br2 , 溴水溶液的颜色是橙色的;故答案为:蓝色;2I﹣+Cl2═2Cl﹣+I2;橙色;(5)因为Cl2有毒,所以氯气需要用碱液吸收,又因为在水中的溶解度不大,故不需防倒吸;故答案为:B.(1)分析装置图中仪器作用和图形写出名称,注意区分普通漏斗、分液漏斗和长颈漏斗三种漏斗在结构上的不同,注意圆底烧瓶、平底烧瓶和蒸馏烧瓶的区别;(2)洗气装置C是为了除去Cl2中的HCl气体,选择饱和食盐水吸收氯化氢,D是为了干燥Cl2 , 选择浓硫酸干燥氯气,除杂顺序一般是先净化后干燥;(3)依据氯气能使湿润的有色布条褪色,不能使干燥的有色布条褪色;(4)氯气和碘化钾溶液中的碘离子反应生成碘单质.遇到淀粉变蓝,通过溴化钠溶液中的溴离子被氧化为溴单质;(5)氯气有毒污染空气,需要用氢氧化钠溶液吸收,氯气溶解性较小不需要防止倒吸;


科目:高中化学 来源: 题型:
【题目】下列有关物质结构的说法正确的是( )
A.78g Na2O2晶体中所含阴、阳离子个数均为4NA
B.3.4g氨气中含有0.6NA个N﹣H键
C.HBr的电子式为![]()
D.PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 物质的摩尔质量等于其相对分子(或原子)质量
B. 物质的摩尔质量是该物质1 mol时的质量
C. 物质的摩尔质量等于其相对分子质量的6.02×1023倍
D. 摩尔质量的单位是g·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大.其中A原子核外有三个未成对电子; B元素是地壳中含量最多的金属元素;C原子核外的M层中有两对成对电子;D是使用最广泛的合金的主要成分.E原子核外最外层只有1个电子,其余各层电子均充满.请根据以上信息,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)E+离子的最外层电子排布式 , A、B、C的第一电离能最小的是
(2)A的最高价含氧酸分子中心原子是杂化.
(3)A、B形成某种化合物的晶胞结构如下图一所示(“O”表示B原子),则其化学式为 , 一个B原子周围距离最近且等距的B原子有个.B原子的堆积方式与下图中的相同.(填“图二”或“图三”)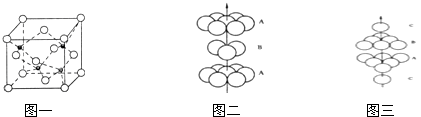
(4)1183K以下D晶体的晶胞为钾型,而1183K以上则转变为铜型,在两种晶胞中最邻近的D原子间距离相同,则两种晶体中原子的空间利用率之比为(可用根号表示).
(5)开发新型储氢材料是氢能利用的重要研究方向.分子X可以通过氢键形成“笼状结构”而成为潜在的储氢材料.X一定不是(填标号).
A.H2O
B.CH4
C.HF
D.CO(NH2)2 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种物质都含有同一元素,它们按如图所示关系相互转化(部分反应物和产物没有标明),已知A为单质,E的俗名为纯碱.
(1)写出化学式:A , B , E .
(2)分别写出相关的化学方程式:A→C:
C→D: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1mol的镁、铝混合物溶于100mL2mol/LH2SO4溶液中,然后再滴加1mol/LNaOH溶液.若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示.当V2=460mL时,则原混合物中镁铝的质量比是( ) 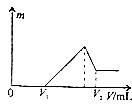
A.1:1
B.2:3
C.16:27
D.8:9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将铁、氧化铁、氧化铜的混合物粉末放入110mL4mol/L盐酸中,充分反应后产生896mLH2(标准状况),残留固体1.00g.过滤,滤液中无Cu2+ . 将滤液加水稀释到200mL,测得其中c(H+)为0.4mol/L.求原混合物的总质量.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com