
在一定温度下,向容积固定不变的密闭容器内充入a mol NO2,发生如下反应:2NO2 (g) N2O4 (g) ,则达到平衡后,再向该容器内充入a mol NO2,达新平衡后与原平衡比较不正确的是 ( )
N2O4 (g) ,则达到平衡后,再向该容器内充入a mol NO2,达新平衡后与原平衡比较不正确的是 ( )
A.平均相对分子质量增大 B.NO2的质量分数增大
C.颜色变深  D.反应放出的总热量大于原平衡的2倍
D.反应放出的总热量大于原平衡的2倍
 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源:2016-2017学年广东佛山一中高二上第一次段考化学卷(解析版) 题型:实验题
为探究测定中和热的实验,小明利用50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液,在如图所示的装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热(中和热数值为57.3 kJ/mol)。
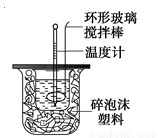
(1)写出实验所进行的中和反应的热化学方程式 。
(2)实验装置中,烧杯间填满碎纸条的作用为  。
。
(3)该实验中,使用浓度略大于盐酸的NaOH溶液的原因是 ,若改用60 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1,NaOH溶液进行反应,所求中和热的数值_________(填“相等”或“不相等”),理由是 。
(4)小明利用上述装置做实验,测得中和热的数值偏低,请你分析可能的原因是 。
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.做本实验的当天室温较高
C.将量筒中的NaOH(aq)倒入小烧杯时动作迟缓
D.在量取盐酸时仰视读数
E.大烧杯的盖板中间小孔太大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东佛山一中高二上第一次段考化学卷(解析版) 题型:选择题
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=+49.0kJ·mol-1
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g);△H=-192.9kJ·mol-1
下列说法正确的是
A.CH3OH的燃烧热为192.9kJ·mol-1
B.反应①中的能量变化如图所示
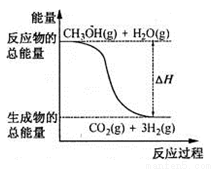
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知反应CH3OH(l)+1/2O2(g)=CO2 (g)+2H2(g)的△H>-192.9kJ·mo
(g)+2H2(g)的△H>-192.9kJ·mo l-1
l-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com