

| A. | 2NH4Cl+Ba(OH)2•H2O═BaCl2+2NH3↑+10H2O | |
| B. | 2HI(g)═H2(g)+I2(g)△H=+14.9 kJ.mol-1 | |
| C. | 形成化学键时共放出能量862 kJ的化学反应 | |
| D. | 能量变化如图所示的化学反应 |
分析 根据常见的放热反应有:所有的物质燃烧、所有金属与酸反应、金属与水反应,所有中和反应;绝大多数化合反应和铝热反应;
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),少数分解置换以及某些复分解(如铵盐和强碱),C或氢气做还原剂时的反应.
解答 解:A.氯化铵和氢氧化钡晶体常温下反应属于吸热反应,故A错误;
B.反应的焓变为正值属于吸热反应,故B错误;
C.化学反应能量变化由断裂化学键吸收的能量和形成化学键放出的能量决定,形成化学键时共放出能量862 kJ的化学反应可能是吸热反应,故C错误;
D.图象中反应物能量高于生成物,反应一定是放热反应,故D正确;
故选D.
点评 本题考查了放热反应的判断,难度不大,抓住中学化学中常见的吸热或放热的反应是解题的关键,对于特殊过程中的热量变化的要熟练记忆来解答此类习题.


科目:高中化学 来源: 题型:解答题
 随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1 4.3×10-7 K2 5.6×10-11 | 3.0×10-8 |
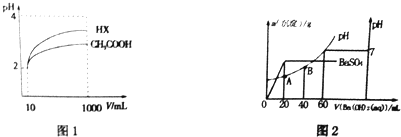
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3-甲基-4-乙基戊烷 | B. | 3,4,4-三甲基己烷 | ||
| C. | 3-甲基-5-己烯 | D. | 3,3-二甲基-1-戊烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

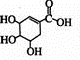 +Br2→
+Br2→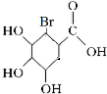 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c (A-)>c (B+)>c (H+)>c (OH-) | B. | c (B+)=c (A-)>c (H+)=c (OH-) | ||
| C. | c (OH-)-c (H+)=c(HA) | D. | c (B+)+c (H+)=c (A-)+c (OH-)+c(HA) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2c=b | B. | c=+285.8 | ||
| C. | 通过原电池可以实现反应(3) | D. | 氢气的燃烧热为a kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
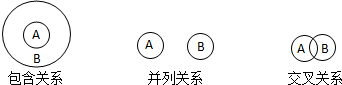
| A. | 纯净物与混合物属于包含关系 | |
| B. | 胶体与分散系属于交叉关系 | |
| C. | 置换反应与离子反应属于交叉关系 | |
| D. | 氧化还原反应与分解反应属于并列关系 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com