
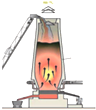
| A£®»š·ØĮ¶Ķ | B£®ÖŠŗĶµĪ¶Ø | C£®Äš¾Ę | D£®ÖĘŅų¾µ |
 |  |  |  |
| A£® | A | B£® | B | C£® | C | D£® | D |
·ÖĪö ·“Ó¦ÖŠ“ęŌŚŌŖĖŲµÄ»ÆŗĻ¼Ū±ä»ÆĪŖŃõ»Æ»¹Ō·“Ó¦£¬Čō²»“ęŌŚŌŖĖŲµÄ»ÆŗĻ¼Ū±ä»Æ£¬Ōņ²»ŹōÓŚŃõ»Æ»¹Ō·“Ó¦£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗA£®»š·ØĮ¶Ķ£¬CuŌŖĖŲµÄ»ÆŗĻ¼Ū±ä»Æ£¬ŹōÓŚŃõ»Æ»¹Ō·“Ó¦£¬¹ŹA²»Ń”£»
B£®ÖŠŗĶµĪ¶ØŹ±Ėį¼īÖŠŗĶ·“Ó¦£¬ŹōÓŚø“·Ö½ā·“Ó¦£¬Ć»ÓŠŌŖĖŲµÄ»ÆŗĻ¼Ū±ä»Æ£¬²»Éę¼°Ńõ»Æ»¹Ō·“Ó¦£¬¹ŹBŃ”£»
C£®Äš¾ĘÖŠĮøŹ³·¢½Ķ£¬ÓŠŌŖĖŲµÄ»ÆŗĻ¼Ū±ä»Æ£¬ĪŖŃõ»Æ»¹Ō·“Ó¦£¬¹ŹC²»Ń”£»
D£®ÖĘŅų¾µ£¬AgŌŖĖŲµÄ»ÆŗĻ¼Ū½µµĶ£¬CŌŖĖŲµÄ»ÆŗĻ¼ŪÉżøߣ¬ĪŖŃõ»Æ»¹Ō·“Ó¦£¬¹ŹD²»Ń”£»
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éŃõ»Æ»¹Ō·“Ó¦£¬ĪŖøßæ¼øßĘµæ¼µć£¬°ŃĪÕ·¢ÉśµÄ»Æѧ·“Ó¦¼°·“Ó¦ÖŠŌŖĖŲµÄ»ÆŗĻ¼Ū±ä»ÆĪŖ½ā“šµÄ¹Ų¼ü£¬×¢Ņā“Ó»ÆŗĻ¼Ū½Ē¶Č·ÖĪö£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ū¢Ż | B£® | ¢Ł¢Ż | C£® | ¢Ś¢Ū¢Ż | D£® | ¢Ł¢Ś |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
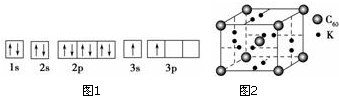 ÄÉĆ×¼¼ŹõÖĘ³ÉµÄ½šŹōČ¼ĮĻ”¢·Ē½šŹō¹ĢĢåČ¼ĮĻ”¢ĒāĘųµČŅŃÓ¦ÓƵ½Éē»įÉś»īŗĶøßæĘ¼¼ĮģÓņ£®µ„Ī»ÖŹĮæµÄAŗĶBµÄµ„ÖŹČ¼ÉÕŹ±¾ł·Å³ö“óĮæČČ£¬æÉÓĆ×÷Č¼ĮĻ£®ŅŃÖŖAŗĶBĪŖ¶ĢÖÜĘŚŌŖĖŲ£¬ĘäŌ×ӵĵŚŅ»ÖĮµŚĖĵēĄėÄÜČēĻĀ±ķĖłŹ¾£ŗ
ÄÉĆ×¼¼ŹõÖĘ³ÉµÄ½šŹōČ¼ĮĻ”¢·Ē½šŹō¹ĢĢåČ¼ĮĻ”¢ĒāĘųµČŅŃÓ¦ÓƵ½Éē»įÉś»īŗĶøßæĘ¼¼ĮģÓņ£®µ„Ī»ÖŹĮæµÄAŗĶBµÄµ„ÖŹČ¼ÉÕŹ±¾ł·Å³ö“óĮæČČ£¬æÉÓĆ×÷Č¼ĮĻ£®ŅŃÖŖAŗĶBĪŖ¶ĢÖÜĘŚŌŖĖŲ£¬ĘäŌ×ӵĵŚŅ»ÖĮµŚĖĵēĄėÄÜČēĻĀ±ķĖłŹ¾£ŗ| µēĄėÄÜ/£ØkJ•mol-1£© | I1 | I2 | I3 | I4 |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
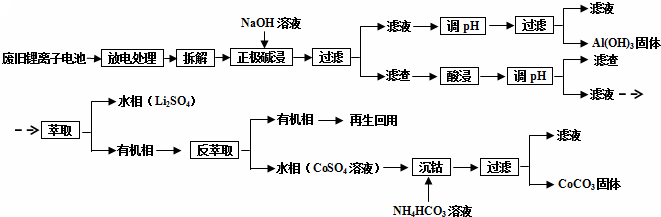
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

| Ź±¼ä/min ĪĀ¶Č/”ę | 0 | 10 | 20 | 40 | 50 |
| T1 | 1.2 | 0.9 | 0.7 | 0.4 | 0.4 |
| T2 | 1.2 | 0.8 | 0.56 | 0.5 | 0.5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
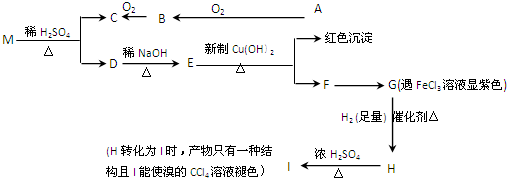
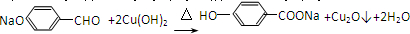 £»
£» £®
£®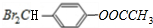 £®
£®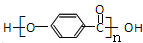 £®
£® £®£ØČĪŠ“Ņ»ÖÖ£©
£®£ØČĪŠ“Ņ»ÖÖ£©²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ£¬2.24LŅŅ“¼·Ö×ÓĖłŗ¬µÄC-H¼üŹżĪŖ0.5NA | |
| B£® | 3.2æĖO2ŗĶO3µÄ»ģŗĻĘųÖŠŗ¬ÓŠµÄŃõŌ×ÓŹżÄæĪŖ0.2NA | |
| C£® | 0.1mol•L-1µÄAl2£ØSO4£©3ČÜŅŗÖŠ£¬AL3+µÄŹżÄæŠ”ÓŚ0.2NA | |
| D£® | 0.1molFe²Ī¼ÓŃõ»Æ»¹Ō·“Ó¦£¬×ŖŅʵĵē×ÓŹżÄæŅ»¶ØŹĒ0.3NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
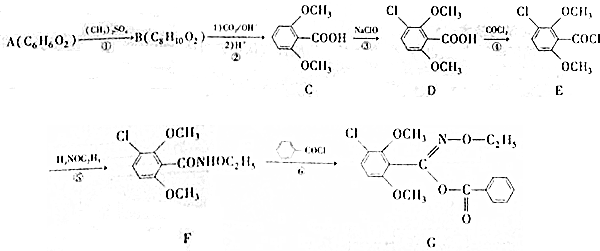
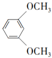 £»¢ŻµÄ·“Ó¦ĄąŠĶĪŖČ”“ś·“Ó¦£®
£»¢ŻµÄ·“Ó¦ĄąŠĶĪŖČ”“ś·“Ó¦£®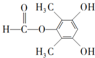 ”¢
”¢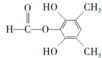 £®
£® ĪŖŌĮĻÖʱø
ĪŖŌĮĻÖʱø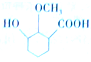 µÄŗĻ³ÉĀ·Ļß
µÄŗĻ³ÉĀ·Ļß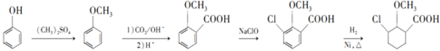
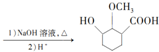
 £ØĪŽ»śŹŌ¼ĮæÉČĪŃ”£©
£ØĪŽ»śŹŌ¼ĮæÉČĪŃ”£©²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com