
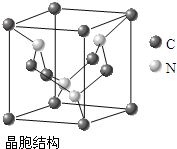
 [化学-物质结构与性质]
[化学-物质结构与性质]| A-B | A=B | A≡B | |
| CO | 357.7 | 798.9 | 1071.9 |
| N2 | 154.8 | 418.4 | 941.7 |
| 1 |
| 8 |
| 1 |
| 2 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
A、亚硫酸氢铵溶液与含等物质的量的NaOH的溶液混合:N
| |||||||||||||||
B、氢氧化钡溶液与硫酸氢钠溶液反应至溶液恰好呈中性:Ba2++2H++SO42-+2OH-
| |||||||||||||||
C、向明矾[KAl(SO4)2]溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全:2Al3++3SO42-+3Ba2++6OH-
| |||||||||||||||
D、向碳酸氢镁溶液中加入过量澄清石灰水:Mg2++2HC
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| ||
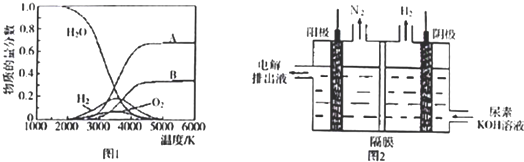
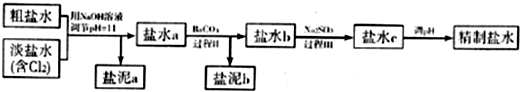
查看答案和解析>>
科目:高中化学 来源: 题型:
A、遇Fe(CN)
| ||||
B、水电离出c(OH-)>10-5mol?L-1;Mg2+、Cl-、NO
| ||||
C、遇石蕊变红的溶液:Na+、NH
| ||||
D、与铝反应产生大量氢气的溶液:Ba2+、HCO
|
查看答案和解析>>
科目:高中化学 来源: 题型:
 近年来,化学工作者在CO2的应用研究上取得了一些重要成果.
近年来,化学工作者在CO2的应用研究上取得了一些重要成果.| 3 |
| 2 |
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| 已知 | 类推 | |||||||||
| A | 将Fe加入CuSO4溶液中:Fe+Cu2+=Cu+Fe2+ | 将Na加入到CuSO4溶液中:2Na+Cu2+=Cu+2Na+ | ||||||||
| B | 稀硫酸与Ba(OH)2溶液反应至溶液呈中性:2H++SO42-+Ba++2OH-=BaSO4↓+2H2O | NaHSO4溶液与Ba(OH)2溶液反应呈中性:2H++SO42-+Ba++2OH-=BaSO4↓+2H2O | ||||||||
| C | 铁和氯气反应2Fe+3Cl2
|
铁和单质反应2Fe+3I2
| ||||||||
| D | 向Ca(ClO)2溶液中通入少量CO2:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO | 向Ca(ClO)2溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| A、反应①②都是氧化还原反应 |
| B、反应②是置换反应 |
| C、反应①中Ti02:是氧化剂 |
| D、反应②中每生成1mol Ti转移4 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
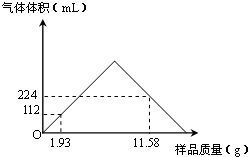 含钡化合物在实验室和工业生产中都有广泛的用途.
含钡化合物在实验室和工业生产中都有广泛的用途.| 500-520℃ |
| 1 |
| 9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com