
 工业合成氨反应为:N2(g)+3H2(g) $?_{高温高压}^{催化剂}$ 2NH3(g),对其研究如下:
工业合成氨反应为:N2(g)+3H2(g) $?_{高温高压}^{催化剂}$ 2NH3(g),对其研究如下:| t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| n(H2)/mol | 6.00 | 4.50 | 3.60 | 3.30 | 3.03 | 3.00 | 3.00 |
| n(NH3)/mol | 0 | 1.00 | 1.60 | 1.80 | 1.98 | 2.00 | 2.00 |
分析 (1)根据反应热=反应物的总键能-生成物的总键能,据此计算;
(2)K为生成物浓度幂之积与反应物浓度幂之积的比,化学计量数为倍数关系,而K为指数关系;
(3)①由表可知表可知25min反应达平衡状态,
N2(g)+3H2(g)?2NH3(g),
初起(mol/L):2 6 0
变化(mol/L):1 3 2
平衡(mol/L):1 3 2
此时平衡常数为:K=$\frac{{2}^{2}}{{3}^{3}×1}$=$\frac{4}{27}$,根据Qc与K的大小平衡判断正逆反应速率的大小;
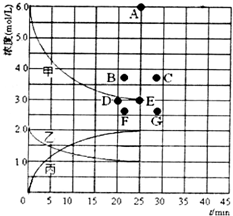
②由反应方程式可知:N2(g)+3H2(g)?2NH3(g)变化量之比等于对应物质的化学计量数之比,而△n甲:△n乙:△n丙=3:1:2,所以表示c(N2)~t的曲线是乙;在此温度下,若起始充入4molN2和12molH2,相当于在原来基础上增加压强,平衡正向移动,所以比原平衡的两倍小,而且达平衡的时间缩短,由此分析解答.
解答 解:(1)已知:H-H键能为436kJ•mol-1,H-N键能为391kJ•mol-1,N≡N键的键能945.6kJ•mol-1,对于反应N2(g)+3H2(g)=2NH3(g)的反应热=反应物的总键能-生成物的总键能=945.6kJ•mol-1+436kJ•mol-1×2-391kJ•mol-1×6=-92.46kJ•mol-1,
故答案为:-92.46kJ•mol-1;
(2)N2(g)+3H2(g) $?_{高温高压}^{催化剂}$ 2NH3(g)的K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}){c}^{3}({H}_{2})}$,$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)?NH3(g),在该温度下的平衡常数:K1=$\sqrt{K}$,
故答案为:$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}){c}^{3}({H}_{2})}$;$\sqrt{K}$;
(3)①由表可知表可知25min反应达平衡状态,
N2(g)+3H2(g)?2NH3(g),
初起(mol/L):2 6 0
变化(mol/L):1 3 2
平衡(mol/L):1 3 2
此时平衡常数为:K=$\frac{{2}^{2}}{{3}^{3}×1}$=$\frac{4}{27}$,根据Qc=$\frac{{3}^{2}}{{3}^{3}×3}$=$\frac{3}{27}$<K,所以平衡正向移动,即此时v正大于v逆,
故答案为:大于;
②由反应方程式可知:N2(g)+3H2(g)?2NH3(g)变化量之比等于对应物质的化学计量数之比,而△n甲:△n乙:△n丙=3:1:2,所以表示c(N2)~t的曲线是乙;在此温度下,若起始充入4molN2和12molH2,相当于在原来基础上增加压强,平衡正向移动,所以比原平衡的两倍小,而且达平衡的时间缩短,则应是点B,
故答案为:乙;B.
点评 本题考查化学平衡的计算,为高频考点,把握图象及表格数据的应用、平衡三段法、K与Qc的计算为解答的关键,侧重分析与计算能力的考查,注意焓变计算方法、平衡移动原理的应用,题目难度不大.


科目:高中化学 来源:2016-2017学年四川省高二上10月月考化学试卷(解析版) 题型:选择题
水煤气反应C(s)+H2O(g)?CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率增大的是
A.增加C的量
B.将容器的体积缩小一半
C.保持体积不变,充入N2使体系压强增大
D.保持体积不变,将生成的H2及时移出容器
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西西藏民族学院附中高二上月考二化学卷(解析版) 题型:实验题
(1)如图分别是温度计、量筒、滴定管的一部分,则:温度计应该是 ,读数是_______℃;量筒应该是 ,读数为 mL;滴定管应该是 ,读数为 mL 。



(2)用已知浓度的盐酸滴定未知浓度的氢氧化钠溶液时,下列实验操作会引起测量结果偏高的是 。
①读取滴定管终点读数时,仰视刻度线。
②滴定前滴定管尖嘴有气泡,滴定后尖嘴气泡消失
③中和滴定时,锥形瓶内有少量蒸馏水。
④酸式滴定管用蒸馏水洗后,未用标准液洗。
⑤用天平称量NaOH固体,将小烧杯放在右盘,砝码放在左盘,并移动游码,使之平衡。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西西藏民族学院附中高二上月考二化学卷(解析版) 题型:选择题
化学电池可以直接将化学能转化为电能,化学电池的本质是( )
A.化合价的升降 B.电子的转移 C.氧化还原反应 D.电能的储存
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西西藏民族学院附中高二上月考二化学卷(解析版) 题型:选择题
已知反应X+Y= M+N为放热反应,,对该反应的下列说法中正确的( )
A. X的能量一定高于M
B. Y的能量一定高于N
C. X和Y的总能量一定高于M和N的总能量
D. 因该反应为放热反应,故不必加热就可发生
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4.68 g | B. | 6..68 g | ||
| C. | 2.34 g | D. | 由于m未知,无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
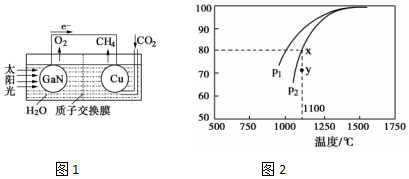 天然气是一种重要的清洁能源和化工原料,其主要成分为甲烷.
天然气是一种重要的清洁能源和化工原料,其主要成分为甲烷.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com