
【题目】对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。
(1)含氰废水中的CN-有剧毒。在微生物的作用下,CN-能够被氧气氧化成HCO3-,同时生成NH3,该反应的离子方程式为_______。
(2)高铁酸钠(Na2FeO4)是一种多功能、高效无毒的新型绿色水处理剂。
① Na2FeO4中铁元素的化合价是______价。
② 用Na2FeO4给水消毒、杀菌时得到的Fe3+可以净水,Fe3+净水原因是_______(用离子方程式表示)。
③ 工业上可用FeCl3、NaOH 、NaClO三种物质在一定条件下反应制得Na2FeO4,完成下列化学方程式:2FeCl3 +10NaOH+3NaClO=2_____+5_____+9_______。
【答案】2CN-+4H2O+O2 ![]() 2HCO3-+2NH3+6Fe3++3H2O
2HCO3-+2NH3+6Fe3++3H2O ![]() Fe(OH)3+3H+Na2FeO4H2ONaCl
Fe(OH)3+3H+Na2FeO4H2ONaCl
【解析】
本题考查氧化还原反应。
(1)由题意可知,在微生物的作用下,CN-能够被氧气氧化成HCO3-,同时生成NH3,反应的离子方程式为:2CN-+4H2O+O2![]() 2HCO3-+2NH3。(2)设Na2FeO4中铁元素的化合价为x,由化合价代数和为0可得:+1×2+x+(-2)×4=0,解得x=+6;Fe3+是弱碱阳离子,能水解生成Fe(OH)3胶体,Fe(OH)3胶体,可以吸附水中悬浮物并凝聚沉降达到净水的目的,Fe3+水解的离子方程式为:Fe3++3H2O
2HCO3-+2NH3。(2)设Na2FeO4中铁元素的化合价为x,由化合价代数和为0可得:+1×2+x+(-2)×4=0,解得x=+6;Fe3+是弱碱阳离子,能水解生成Fe(OH)3胶体,Fe(OH)3胶体,可以吸附水中悬浮物并凝聚沉降达到净水的目的,Fe3+水解的离子方程式为:Fe3++3H2O![]() Fe(OH)3+3H+;由于是用FeCl3、NaOH、NaClO三种物质在一定条件下反应制得Na2FeO4,故2mol FeCl3失去6mol电子,被氧化为2molNa2FeO4,失去的6mol电子能被3molNaClO得到,NaClO中+1价氯元素还原为-1价,得3molCl-,加上2molFeCl3中的6molCl-,一共会生成9molNaCl,反应物中有10molNaOH,根据氢原子的守恒可知,产物中会生成5molH2O。
Fe(OH)3+3H+;由于是用FeCl3、NaOH、NaClO三种物质在一定条件下反应制得Na2FeO4,故2mol FeCl3失去6mol电子,被氧化为2molNa2FeO4,失去的6mol电子能被3molNaClO得到,NaClO中+1价氯元素还原为-1价,得3molCl-,加上2molFeCl3中的6molCl-,一共会生成9molNaCl,反应物中有10molNaOH,根据氢原子的守恒可知,产物中会生成5molH2O。


 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:高中化学 来源: 题型:
【题目】向X溶液中缓慢滴加Y溶液,生成沉淀的质量如图所示,符合图像的一组是

X | Y | |
A | AlCl3、Mg(NO3)2、HNO3 | NaOH |
B | Na2CO3、NH4HCO3、Na2SO4 | Ba(OH)2 |
C | NH4NO3、Al(NO3)3、Fe(NO3)3、HCl | NaOH |
D | NaAlO2、氨水、NaOH | H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚维酮碘的水溶液是一种常用的碘伏类缓释消毒剂,聚维酮通过氢键与HI3形成聚维酮碘,其结构表示如下: (图中虚线表示氢键),下列说法不正确的是
(图中虚线表示氢键),下列说法不正确的是
A. 合成聚维酮的单体有二种 B. 聚维酮分子由(2m+n)个单体聚合而成
C. 聚维酮碘是一种水溶性物质 D. 聚维酮是加聚反应的产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列四种烃的有关说法正确的是
①![]() ②
②
③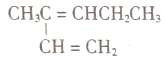 ④
④
A. ①催化加氢可生成3-甲基已烷 B. ③与④催化加氢后的产物质谱图完全一样
C. ③中所有碳原子有可能共平面 D. ②在同一直线上的碳原子有5个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】针对下列9种元素,完成以下各小题
周期 | IA | ⅡA | ⅢA | ⅣA | ⅥA | ⅦA | O | |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)常见单质为有色气体的元素是_______(填名称)。
(2)用电子式表示元素④和⑨形成化合物的过程_________。
(3)最高价氧化物对应的水化物中酸性最强的是_________(填化学式)。
(4)④和⑥两者的最高价氧化物对应的水化物反应的离子方程式为_______。
(5)⑦的单质的用途正确的是_____。
A.光导纤维 B.太阳能电池 C.普通玻璃 D.计算机芯片
(6)元素①和⑦非金属性较强的是____(填写元素符号),写出一个能表示二者非金属性强弱关系的化学方程式为:_______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)锌锰干电池是应用最普遍的电池之一(如图所示),锌锰干电池的负极材料是____,负极发生的电极反应方程式为:____。若反应消耗32.5 g 负极材料,则电池中转移电子的数目为____。

(2)目前常用的镍(Ni)镉(Cd)电池其电池总反应式可以表示为:Cd+2NiO(OH)+2H2O![]() 2Ni(OH)2+Cd(OH)2,(充电是指外加电流作用发生氧化还原反应)已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法中正确的是____。
2Ni(OH)2+Cd(OH)2,(充电是指外加电流作用发生氧化还原反应)已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法中正确的是____。
①上述反应可以在酸性条件下进行 ②上述反应不是可逆反应
③放电时正极金属Cd的质量增加 ④放电时化学能转变为电能
(3)如图为氢氧燃料电池的构造示意图,电解质溶液的溶质是KOH。则X极为电池的_____(填“正”或“负”)极,X极的电极反应方程为_______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中正确的是( )
①CS2为V形的极性分子 ②ClO![]() 的空间构型为平面三角形
的空间构型为平面三角形
③SF6中有6对完全相同的成键电子对 ④SiF4和SO![]() 的中心原子均为sp3杂化
的中心原子均为sp3杂化
A. ①② B. ②③ C. ③④ D. ④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在合成氨反应中,将等物质的量的氮气和氢气充入一密闭容器中发生反应,测得 2min 内氨的平均反应速率为 2 mol·L-1·min -1,2min 末 N2 的浓度为7 mol·L-1,则氢气的起始浓度为
A.9 mol·L-1
B.6 mol·L-1
C.3 mol·L-1
D.2 mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com