
 CO£Øg£©£«H2O£Øg£©£¬
CO£Øg£©£«H2O£Øg£©£¬| t”ę | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
 ÖĒȤŹī¼ŁĪĀ¹ŹÖŖŠĀĻµĮŠ“š°ø
ÖĒȤŹī¼ŁĪĀ¹ŹÖŖŠĀĻµĮŠ“š°ø Ó¢ÓļŠ”Ó¢ŠŪĢģĢģĬŠ“ĻµĮŠ“š°ø
Ó¢ÓļŠ”Ó¢ŠŪĢģĢģĬŠ“ĻµĮŠ“š°ø Źī¼Ł×÷Ņµ°²»ÕÉŁÄź¶łĶƳö°ęÉēĻµĮŠ“š°ø
Źī¼Ł×÷Ņµ°²»ÕÉŁÄź¶łĶƳö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
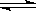 2C(g)“ļµ½Ę½ŗā£¬“ĖŹ±²āµĆn(A)”Ćn(B)”Ćn(C)=2”Ć2”Ć1”£Čō±£³ÖĪĀ¶Č²»±ä£¬ŅŌn(A)”Ćn(B)”Ćn(C)=2”Ć2”Ć1µÄ±ČĄżĻņøĆČŻĘ÷ÖŠŌŁ³äČėA”¢BŗĶC£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
2C(g)“ļµ½Ę½ŗā£¬“ĖŹ±²āµĆn(A)”Ćn(B)”Ćn(C)=2”Ć2”Ć1”£Čō±£³ÖĪĀ¶Č²»±ä£¬ŅŌn(A)”Ćn(B)”Ćn(C)=2”Ć2”Ć1µÄ±ČĄżĻņøĆČŻĘ÷ÖŠŌŁ³äČėA”¢BŗĶC£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
 xC£Øg£©£«2D£Øs£©£¬2minŹ±·“Ó¦“ļµ½Ę½ŗāדĢ¬£®“ĖŹ±Ź£Óą1.2mol B£¬²¢²āµĆCµÄÅضČĪŖ1
xC£Øg£©£«2D£Øs£©£¬2minŹ±·“Ó¦“ļµ½Ę½ŗāדĢ¬£®“ĖŹ±Ź£Óą1.2mol B£¬²¢²āµĆCµÄÅضČĪŖ1 £®2mol”¤L£1”£
£®2mol”¤L£1”£²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
 C(g) “ļµ½Ę½ŗāŹ±£¬CµÄĢå»ż·ÖŹżĪŖ40£„”£ŹŌ»Ų“šÓŠ¹ŲĪŹĢā£ŗ
C(g) “ļµ½Ę½ŗāŹ±£¬CµÄĢå»ż·ÖŹżĪŖ40£„”£ŹŌ»Ų“šÓŠ¹ŲĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
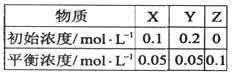

| A£®·“Ó¦“ļµ½Ę½ŗāŹ±£¬XµÄ×Ŗ»ÆĀŹĪŖ50£„ |
B£®·“Ó¦æɱķŹ¾ĪŖX+3Y 2Z£¬ĘäĘ½ŗā³£ŹżĪŖ1600 2Z£¬ĘäĘ½ŗā³£ŹżĪŖ1600 |
| C£®Ōö“óŃ¹ĒæŹ¹Ę½ŗāĻņÉś³ÉZµÄ·½ĻņŅĘ¶Æ£¬Ę½ŗā³£ŹżŌö“ó |
| D£®øıäĪĀ¶ČæÉŅŌøıä“Ė·“Ó¦µÄĘ½ŗā³£Źż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 nC£Øg£©£Ø”÷H<0£©ŌŚ²»Ķ¬Ģõ¼žĻĀ·“Ó¦»ģŗĻĪļÖŠCµÄĢå»ż·ÖŹżÓė·“Ó¦¹ż³ĢĖłŠčŹ±¼äµÄ¹ŲĻµĒśĻß”£ŌņĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ
nC£Øg£©£Ø”÷H<0£©ŌŚ²»Ķ¬Ģõ¼žĻĀ·“Ó¦»ģŗĻĪļÖŠCµÄĢå»ż·ÖŹżÓė·“Ó¦¹ż³ĢĖłŠčŹ±¼äµÄ¹ŲĻµĒśĻß”£ŌņĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ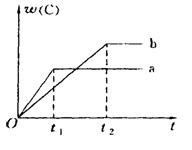
| A£®a±ķŹ¾ÓŠ“߻ƼĮ£¬b±ķŹ¾ĪŽ“߻ƼĮ |
| B£®ČōĘäĖūĢõ¼žĻąĶ¬£¬a±ČbµÄĪĀ¶ČµĶ |
| C£®·“Ó¦ÓÉÕż·“Ó¦æŖŹ¼ |
| D£®·“Ó¦ÓÉÄę·“Ó¦æŖŹ¼ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
 2NO2£Øg£© ”÷H>0 £¬ŌŚĪĀ¶ČĪŖT1”¢ T2Ź±£¬Ę½ŗāĢåĻµÖŠNO2µÄĢå»ż·ÖŹżĖęŃ¹Ēæ±ä»ÆĒśĻßČēĶ¼ĖłŹ¾”£T1 T2£ØĢī”°>”±”¢”°<”±»ņ”°=”±£©£»A”¢CĮ½µćµÄĖŁĀŹvA vC£Ø
2NO2£Øg£© ”÷H>0 £¬ŌŚĪĀ¶ČĪŖT1”¢ T2Ź±£¬Ę½ŗāĢåĻµÖŠNO2µÄĢå»ż·ÖŹżĖęŃ¹Ēæ±ä»ÆĒśĻßČēĶ¼ĖłŹ¾”£T1 T2£ØĢī”°>”±”¢”°<”±»ņ”°=”±£©£»A”¢CĮ½µćµÄĖŁĀŹvA vC£Ø Ķ¬ÉĻ£©”£
Ķ¬ÉĻ£©”£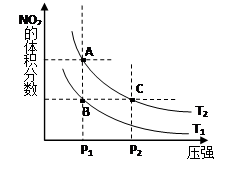
| Ź±¼ä£Øs£© | 0 | 20 | 40 | 60 | 80 |
| n£ØNO2£©/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n£ØN2O4£©/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 N2O4Ę½ŗā£¬Ę½ŗāŹ±NO2ÓėN2O4ĪļÖŹµÄĮæÅضČÖ®±ČĪŖ¦µ£¬Ģõ¼ž²»±äµÄĒé
N2O4Ę½ŗā£¬Ę½ŗāŹ±NO2ÓėN2O4ĪļÖŹµÄĮæÅضČÖ®±ČĪŖ¦µ£¬Ģõ¼ž²»±äµÄĒé æöĻĀ£¬·Ö±šŌŁ³äČėNO2ŗĶŌŁ³äČėN2O4£¬Ę½ŗāŗó»įŅżĘš¦µµÄ±ä»ÆÕżČ·µÄŹĒ£ŗ
æöĻĀ£¬·Ö±šŌŁ³äČėNO2ŗĶŌŁ³äČėN2O4£¬Ę½ŗāŗó»įŅżĘš¦µµÄ±ä»ÆÕżČ·µÄŹĒ£ŗ| A£®¶¼ŅżĘš¦µŌö“ó | B£®³äČėNO2ŅżĘš¦µŌö“󣬳äČėN2O4ŅżĘš¦µ¼õŠ” |
| C£®¶¼ŅżĘš¦µ¼õŠ” | D£®³äČėNO2ŅżĘš¦µ¼õŠ”£¬³äČėN2O4ŅżĘš¦µŌö“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 PCl5 (g)
PCl5 (g)| A£®0.15 mol | B£®0.2 mol | C£®0.24 mol | D£®0.48 mol |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com