
【题目】现有两组物质的熔点数据如表所示:

根据表中数据回答下列问题。
(1)A组属于________晶体,其熔化时克服的微粒间的作用力是____________。
(2)B组中HF熔点反常是由于__________。
(3)B组晶体不可能具有的性质是________________。
①硬度小 ②水溶液能导电 ③固体能导电 ④液体状态能导电
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
【题目】我国的纳米基础研究能力已跻身于世界前列,曾制得一种合成纳米材料,其化学式为RN(N为氮元素,且为-3价)。已知该化合物中的Rn+核外有28个电子,则R元素位于元素周期表的( )
A.第3周期第ⅤA族B.第4周期第ⅢA族
C.第5周期第ⅢA族D.第4周期第ⅤA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10mL 0.2mol/L草酸溶液中逐滴加入等浓度的NaOH溶液,溶液中各微粒的物质的量与混合溶液pH的关系如图所示,下列说法正确的是

A. 当V(NaOH溶液)<10mL时,溶液中可能存在:c(Na+)=2c(C2O42-)+c(HC2O4-)
B. 当V(NaOH溶液)=10mL时,溶液中水的电离程度比纯水大
C. 当V(NaOH溶液)=15mL时,溶液中存在: c(Na+)>c(HC2O4-)>c(C2O42-)
D. 当V(NaOH溶液)=20mL时,溶液中存在:c(OH-)=2c(H2C2O4)+c(H+)+c(HC2O4-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴化钠、氯化钠和氧化镁等离子晶体的核间距和晶格能(部分)如下表所示

(1)溴化钠晶体比氯化钠晶体晶格能________(填“大”或“小”),主要原因是_____。
(2)氧化镁晶体比氯化钠晶体晶格能大,主要原因是_________________________________。
(3)溴化钠、氯化钠和氧化镁晶体中,硬度最大的是________。工业制取单质镁时,往往电解的是氯化镁而不是氧化镁,主要原因是_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题.

(1)指出图中明显的错误________________;________________;
(2)A仪器的名称是________________;B仪器的名称是________________;
(3)萃取、分液实验中所用主要玻璃仪器的名称是________________,静置后分液的第一步操作是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将pH均为3,体积均为V0的HA和HB溶液,分别加水稀释至体积V,pH随1g![]() 的变化如右图所示。下列说法正确的是
的变化如右图所示。下列说法正确的是
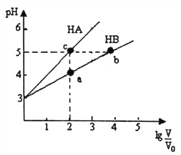
A. 稀释相同倍数时:c(Aˉ)>c(Bˉ-)
B. 水的电离程度:b=c>a
C. 溶液中离子总物质的量:b>c>a
D. 溶液中离子总浓度:a>b>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分。完成下列填空:
IA | IIA | IIIA | IVA | VA | VIA | VIIA | ||
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ |
(1)表中元素,原子半径最大的是_____(填写元素符号);原子核外有两个未成对电子的元素是_____________(填写编号);③和⑥两元素形成化合物的电子式为__________。
(2)⑥⑦两种元素最高价氧化物对应的水化物中,酸性最强的是__________(填化学式)。
(3)比③、④、⑤三种元素的简单离子半径: > > (填离子符号________;元素④最高价氧化物对应的水化物与硫酸反应的离子方程式为________________________。
(3)用一个化学方程式来证明元素②比元素⑥的非金属性强__________________________。
(4)③和⑥两元素形成的化合物溶于水,其溶液中离子浓度由大到小的顺序:__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com