
【题目】[化学——选修3:物质结构与性质](15分)
钾和碘的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为_______nm(填标号)。
A.404.4 B.553.5 C.589.2 D.670.8 E.766.5
(2)基态K原子中,核外电子占据的最高能层的符号是_________,占据该能层电子的电子云轮廓图形状为___________。K和Cr属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属Cr低,原因是___________________________。
(3)X射线衍射测定等发现,I3AsF6中存在I3+离子。I3+离子的几何构型为_____________,中心原子的杂化形式为________________。
(4)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。K与O间的最短距离为______nm,与K紧邻的O个数为__________。
(5)在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于______位置,O处于______位置。

【答案】(1)A (2)N 球形 K的原子半径较大且价电子数较少,金属键较弱
(3)V形 sp3 (4)0.315 12 (5)体心 棱心
【解析】(1)紫色波长400nm~435nm,因此选项A正确;(2)K位于第四周期IA族,电子占据最高能层是第四层,即N层,最后一个电子填充子在s能级上,电子云轮廓图为球形;K的原子半径大于Cr的半径,且价电子数较少,金属键较弱,因此K的熔点、沸点比Cr低;(3)I3+与OF2互为等电子体,OF2属于V型,因此I3+几何构型为V型,其中心原子的杂化类型为sp3;(4)根据晶胞结构,K与O间的最短距离是面对角线的一半,即为![]() =0.315nm,根据晶胞的结构,距离K最近的O的个数为12个;(5)根据KIO3的化学式,以及晶胞结构,K处于体心,O处于棱心。
=0.315nm,根据晶胞的结构,距离K最近的O的个数为12个;(5)根据KIO3的化学式,以及晶胞结构,K处于体心,O处于棱心。


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:
【题目】根据下列反应流程填空:
已知:A是烯烃中分子量最小的,可做果实的催熟剂; C中每个碳上各有一个羟基;

(1)A的名称是_________ B的名称是_________条件Ⅰ是________________;条件Ⅱ是______________________
(2)填反应类型:B→C___________;D→A __________________A →E______________
(3)写方程式: B→C___________ D→A____________________ A → E______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理来解释的是
A. 将混合气中的氨气液化分离,有利于合成氨的反应
B. 用过量氮气与氢气反应可以提高氢气的转化率
C. 密闭容器中发生反应H2(g)+I2(g)![]() 2HI(g),增大压强时容器中颜色加深
2HI(g),增大压强时容器中颜色加深
D. 加压有利于SO2与O2反应生成SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲用NaOH固体配制l. 0 mol L-1的NaOH溶液240 mL;
(1)配制溶液时,一般可以分为以下几个步骤:
①称量②计算③溶解④倒转摇匀⑤转移⑥洗涤⑦定容⑧冷却
其正确的操作顺序为______________(填写序号)。本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、还有_______________________。
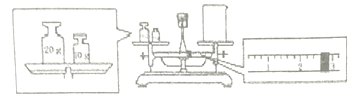
(2)某同学欲称量一定量的NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图。
烧杯的实际质量为___________g,要完成本实验该同学应称出______________g NaOH。
(3)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏高的是____________。
①没有洗涤烧杯和玻璃棒 ②转移溶液时不慎有少量洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水 ④定容时俯视刻度线
⑤未冷却到室温就将溶液转移到容量瓶并定容
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焰火“脚印”、“笑脸”、“五环”,让北京奥运会开幕式更加辉煌、浪漫,这与高中化学中“焰色反应”知识相关。下列说法中正确的是
A. 非金属单质燃烧时火焰均为无色
B. 所有金属及其化合物灼烧时火焰均有颜色
C. 焰色反应均应透过蓝色钴玻璃观察
D. NaC1与Na2CO3灼烧时火焰颜色相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:
CO2(g)+4H2(g)![]() CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
已知H2的体积分数随温度的升高而增加。
若温度从300℃升至400℃,重新达到平衡,判断下列各物理量的变化。(选填“增大”、“减小”或“不变”)v正_______ v逆____________,平衡常数K_______________,转化率α______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[2017海南]已知反应CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH<0。在一定温度和压强下于密闭容器中,反应达到平衡。下列叙述正确的是
CO2(g)+H2(g) ΔH<0。在一定温度和压强下于密闭容器中,反应达到平衡。下列叙述正确的是
A.升高温度,K减小 B.减小压强,n(CO2)增加
C.更换高效催化剂,α(CO)增大 D.充入一定量的氮气,n(H2)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作规范且能达到目的的是
目的 | 操作 | |
A. | 取20.00 mL盐酸 | 在50 mL酸式滴定管中装入盐酸,调整初始读数为30.00mL后,将剩余盐酸放入锥形瓶 |
B. | 清洗碘升华实验所用试管 | 先用酒精清洗,再用水清洗 |
C. | 测定醋酸钠溶液pH | 用玻璃棒蘸取溶液,点在湿润的pH试纸上 |
D. | 配制浓度为0.010 | 称取KMnO4固体0.158 g,放入100 mL容量瓶中,加水溶解并稀释至刻度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com