
分析 依据n=$\frac{m}{M}$=$\frac{N}{N{\;}_{A}}$、m=ρV计算物质的质量,结合物质分子的结构组成解答.
解答 解:A.6g H2物质的量为:$\frac{6g}{2g/mol}$=3mol,含有分子数为:3NA,氢气为双原子分子,所以含有原子个数为:6NA;
B.0.5mol CO2,质量为:0.5mol×44g/mol=22g,含有分子数为:0.5NA,二氧化碳为三原子分子,所以含有原子个数为:1.5NA;
C.148g H2SO4物质的量为:$\frac{148g}{98g/mol}$=1.51mol,含有分子个数:1.51NA,硫酸为6原子分子,所以含有原子个数为:9.06NA;
D.4℃时18mL水,质量为:1g/mL×18mL=18g,物质的量为:$\frac{18g}{18g/mol}$=1mol,含有分子个数为:NA,水分子为三原子分子,则含有原子个数为:3NA;
所以:物质的量最大的是A含分子个数最多的是A含原子个数最多的是C质量最大的是C;
故答案为:A;A; C; C.
点评 本题考查以物质的量为中心的有关计算,熟悉以物质的量为核心计算公式,明确相关物质的结构组成是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| 实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(M) | n(N) | n(P) | ||
| ① | 500 | 0.3 | 0.2 | 0.3 |
| ② | 600 | 0.2 | 0.3 | 0.24 |
| ③ | 750 | 0.1 | 0.1 | x |
| A. | 实验①中,若5 min时测得n(N)=0.050 mol,则0~5min时间内平均反应速率v(P)=0.015 mo1/(L•min) | |
| B. | 实验②中达到平衡后,增大压强,M的转化率增大,平衡常数不变 | |
| C. | 600℃时该反应的平衡常数K=3.0 | |
| D. | 实验③中,达到平衡时,x<0.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 鉴别己烷、己烯和乙醇,可用溴水 | |
| B. | 乙烯和植物油均能使溴的四氯化碳溶液褪色,且反应原理相同 | |
| C. | 甲苯苯环上的一个氢原子被-C3H6Cl取代,形成的同分异构体有9种 | |
| D. | 1mol分子式为C18H26O5的酯完全水解生成lmol 羧酸和2mol乙醇,该羧酸分子式为C14H18O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图为浓硫酸与铜片反应的装置.请回答:
如图为浓硫酸与铜片反应的装置.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 44.Og14CO2与14N2O的混合物中所含中子数为22NA | |
| B. | 标准状况下,2.24L甲醛所含o键数目为0.3NA | |
| C. | 常温常压下,4.5gH2O与足量Na2O2反应转移的电子数目为0.5 NA | |
| D. | 50mL 18mol/L硫酸与足量Cu共热,转移的电子数为0.9NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 物质 | 杂质 | 除杂试剂或操作方法 |
| ① | NaCl | BaCl2 | 加入过量的K2CO3溶液,过滤,再加适量的盐酸并加热 |
| ② | FeSO4溶液 | CuSO4 | 加入过量Fe粉,过滤 |
| ③ | CO2 | HCl | 通过盛饱和Na2CO3溶液洗气瓶,再通过盛H2SO4洗气瓶 |
| ④ | 自来水 | 植物油 | 萃取分液 |
| A. | ①④ | B. | ②③ | C. | ①③④ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
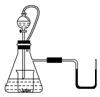 如图所示,若锥形瓶内是水,分液漏斗内的液体也是水,向烧杯内滴加水时,发现U形管内液体慢慢右移,恢复到原温度后液面左边与右边基本相平,则下列说法正确的是( )
如图所示,若锥形瓶内是水,分液漏斗内的液体也是水,向烧杯内滴加水时,发现U形管内液体慢慢右移,恢复到原温度后液面左边与右边基本相平,则下列说法正确的是( )| A. | U型管内液体慢慢向右移动说明将分液漏斗中的水滴入到烧杯中一定发生了化学反应 | |
| B. | U型管内液体慢慢向右移动是由于锥形瓶中气体的总物质的量增大造成压强增大而引起 | |
| C. | 该装置中连接分液漏斗和锥形瓶的橡胶管对于上述实验现象而言其实是可有可无的 | |
| D. | 小烧杯中的物质可以是NaOH也可以是Na2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:2 | B. | 2:1 | C. | 2:5 | D. | 5:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaH是还原剂 | B. | NaH是氧化剂 | ||
| C. | H2O是还原剂 | D. | H2O既不是氧化剂又不是还原剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com