
| A. | 0.4mol氧气 | B. | 4℃时,5.4mLH2O | ||
| C. | 标准状况下5.6L二氧化碳 | D. | 10g氖 |
分析 根据m=ρV计算水的质量,再根据n=$\frac{m}{M}$计算水、氖的物质的量,根据n=$\frac{V}{{V}_{m}}$计算二氧化碳的物质的量,再根据化学式计算各物质含有原子总物质的量,由N=nNA可知,原子物质的量越大,含有原子数目越多.
解答 解:A.0.4mol氧气中含有氧原子物质的量=0.4mol×2=0.8mol;
B.5.4mLH2O的质量=5.4mL×1g/mL=5.4g,其物质的量=$\frac{5.4g}{18g/mol}$=0.3mol,含有原子总物质的量=0.3mol×3=0.9mol;
C.标况下,5.6L二氧化碳的物质的量=$\frac{5.6L}{22.4L/mol}$=0.25mol,含有原子总物质的量=0.25mol×3=0.75mol;
D.10g氖的物质的量=$\frac{10g}{20g/mol}$=0.2mol,为单原子分子,含有原子物质的量为0.2mol,
由N=nNA可知,原子物质的量越大,含有原子数目越多,故5.4mLH2O含有原子数目最多,
故选B.
点评 本题考查微粒数目的有关计算,比较基础,注意理解化学式表示的意义,注意稀有气体为单原子分子.


科目:高中化学 来源: 题型:填空题
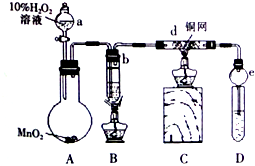 某校课外活动小组的同学在完成课本乙醇氧化制乙醛的实验后,改进了实验方案(如图),进行如下实验操作(顺序已打乱):
某校课外活动小组的同学在完成课本乙醇氧化制乙醛的实验后,改进了实验方案(如图),进行如下实验操作(顺序已打乱):查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液的物质的量浓度:c(KNO3)=$\frac{a}{101V}$mol•L-1 | |
| B. | 该溶液的质量分数:w(KNO3)=$\frac{100a}{a+b}$% | |
| C. | 20℃时KNO3的溶解度S=$\frac{100a}{b}$ g | |
| D. | 该溶液的密度ρ=$\frac{1000(a+b)}{V}$g•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 燃料在火箭发动机中燃烧是将化学能主要转变为热能和机械能 | |
| B. | 偏二甲基肼在四氧化氮中的燃烧反应是放热反应 | |
| C. | 该反应中偏二甲基肼和四氧化氮总能量小于二氧化碳、氮气和水的总能量 | |
| D. | 燃烧时的总反应为:C2H8N2+2N2O4$\stackrel{点燃}{→}$2CO2+3N2+4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室排放的SO2 | B. | 火山爆发产生的SO2 | ||
| C. | 燃烧煤和石油产品产生的SO2 | D. | 工业制硫酸排放的SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 150mL1mol•L-1 NaCl溶液 | B. | 75 mL 0.5mol•L-1 CaCl2溶液 | ||
| C. | 150mL2mol•L-1 KCl溶液 | D. | 75 mL 1 mol•L-1 AlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
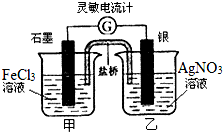 控制适合的条件,将反应Fe3++Ag?Fe2++Ag+设计成如右图所示的原电池,(盐桥装有琼脂-硝酸钾溶液;灵敏电流计的0刻度居中,左右均有刻度)已知,接通后,观察到电流计指针向右偏转.下列判断正确的是( )
控制适合的条件,将反应Fe3++Ag?Fe2++Ag+设计成如右图所示的原电池,(盐桥装有琼脂-硝酸钾溶液;灵敏电流计的0刻度居中,左右均有刻度)已知,接通后,观察到电流计指针向右偏转.下列判断正确的是( )| A. | 在外电路中,电子从石墨电极流向银电极 | |
| B. | 盐桥中的K+移向乙烧杯 | |
| C. | 一段时间后,电流计指针反向偏转,越过0刻度,向左边偏转 | |
| D. | 电流计指针居中后,往甲烧杯中加入一定量的铁粉,电流计指针将向左偏转 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.5p mol | B. | (3m+n/2)mol | C. | (3m+n)mol | D. | (3m+n/2-3 p)mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com