
写出除去下列气体中混有的杂质(括号内为杂质)可采取的方法:
(1)CO(CO2):__________________________________________________________。
(2)CO2(CO):__________________________________________________________。
(3)CO2(O2):__________________________________________________________。
(4)CO2(SO2):_________________________________________________________。
(5)CO2(HCl):_________________________________________________________。
科目:高中化学 来源: 题型:
A、B、C、D、E均为易溶于水的化合物,其离子组成如下。(各化合物中离子组成不重复)
| 阳离子 | Na+、Al3+、Ag+、Ba2+、Fe3+ |
| 阴离子 | Cl-、CO |
分别取溶液进行如下实验:
①用pH试纸分别测得B、C溶液均呈碱性,且0.1 mol/L B溶液pH>13;
②D溶液加入铜粉,溶液质量增加;
③在E溶液中加过量B,没有沉淀产生;
④在A溶液中逐滴滴入氨水至过量,先先成白色沉淀,后沉淀溶解。
请回答下列问题:
(1)B的名称:________,E的名称:________。
(2)C水溶液呈碱性的原因(用离子方程式表示):________;0.1 mol/L的C溶液中和0.1 mol/L的NaHCO3溶液中,阴离子的总数:C溶液________NaHCO3溶液。(填“>”、“=”或“<”)
(3)D溶液呈________(填“酸性”、“碱性”或“中性”);若将D溶液加热蒸干,得到的固体应是:________________________。(填化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
莽草酸是合成治疗禽流感的药物——达菲(Tamiflu)的原料之一。莽草酸是A的一种异构体。A的结构简式如下:
ഠ
(1)A的分子式是 。
(2)A与溴的四氯化碳溶液反应生成物的结构简式是
(3)A与氢氧化钠溶液反应的化学方程式(有机物用结构简式表示)是
(4)17.4克A与足量碳酸氢钠溶液反应,计算生成二氧化碳的体积 (标准状况)。(5)A在浓硫酸作用下加热可得到B(B的结构简式为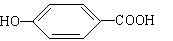 ),其反应类型 。
),其反应类型 。
(6)B的同分异构体中既含有酚羟基又含有酯基的共有 种,写出其中一种同分异构体的结构简式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
强酸和强碱的稀溶液的中和热可表示为:
H+(aq)+OH-(aq)=H2O(1) △H = -57.3kJ/mol
已知:CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(1) △H =- Q1kJ/mol
1/2 H2SO4(浓) + NaOH(aq) == 1/2Na2SO4(aq) +H2O(1) △H =- Q2kJ/mol
HNO3(aq)+KOH(aq)=KNO3(aq)+H2O(1) △H =- Q3kJ/mol
上述反应均为溶液中的反应,则Q1、Q2、Q3的绝对值大小的关系为
A.Q1=Q2=Q3 B.Q2>Q1>Q3 C.Q2>Q3>Q1 D.Q2=Q3>Q1
查看答案和解析>>
科目:高中化学 来源: 题型:
在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂过氧化氢,当它们混合时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量过氧化氢反应,生成氮气和水蒸气,放出 a kJ的热量。
(1) 写出肼和过氧化氢的电子式:肼: ,过氧化氢: ;
(2) 写出该反应的热化学方程式: ;
(3) 已知H2O(1)==H2O(g) △H= + b kJ/mol,则16g液态肼与足量液态过氧化氢反应生成氮气和液态水时,放出的热量是________________ kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
标准状况下,将3.36 L CO2气体通入200 mL 1.00 mol·L-1 NaOH溶液中,充分反应后溶液中c(CO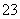 )与 c(HCO
)与 c(HCO )的比值为(不考虑CO
)的比值为(不考虑CO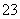 、HCO
、HCO 的水解) ( )
的水解) ( )
A.1∶1 B.1∶2
C.2∶1 D.1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
“碳捕捉技术”是指通过一定的方法将工业生产中产生的CO2分离出 来并利用。如可利用NaOH溶液来“捕捉”CO2,其基本过程如下图所示(部分条件及物质未标出)。
来并利用。如可利用NaOH溶液来“捕捉”CO2,其基本过程如下图所示(部分条件及物质未标出)。

下列有关该方法的叙述中正确的是 ( )
①能耗大是该方法的一大缺点
②整个过程中,只有一种物质可以循环利用
③“反应分离”环节中,分离物质的基本操作是蒸发结晶、过滤
④该方法可减少碳排放,捕捉到的CO2还可用来制备甲醇等产品
A.①② B.②③ C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是
A.Li是最轻的金属,也是活动性极强的金属,是制造电池的理想物质
B.蔗糖、油脂及它们的水解产物均为非电解质
C.海水提取溴、煤的液化、焰色反应都发生了化学变化
D.钢铁在海水中比在河水中更易被腐蚀,主要原因是海水含氧量高
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用下列两种方法制氯气:①用含HCl 146 g的浓盐酸与足量的MnO2反应;②用87 g MnO2与足量浓盐酸反应。所得的氯气 ( )
A.①比②多 B.②比①多
C.一样多 D.无法比较
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com