
| A. | 加热氢氧化钠晶体使之熔化 | B. | 电解水使之分解 | ||
| C. | 碘单质受热升华 | D. | 加热二氧化硅晶体使之熔化 |
科目:高中化学 来源: 题型:推断题
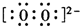 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
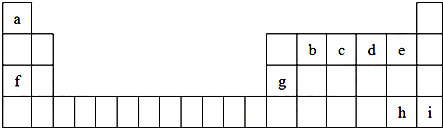
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | -283.01 kJ•mol-1 | B. | +172.51 kJ•mol-1 | ||
| C. | +283.01 kJ•mol-1 | D. | -172.51 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑥ | B. | ②④⑤⑥ | C. | ①③⑤⑥ | D. | 只有④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用氢氧化钠溶液清洗沾有油脂的试管 | |
| B. | 用稀硝酸清洗洁有银镜的试管 | |
| C. | 用水清洗沾有固体石蜡的试管 | |
| D. | 用乙醇清洗沾有苯酚的试管 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非金属元素的原子间不能形成离子化合物 | |
| B. | 所有金属与所有非金属之间都能形成离子键 | |
| C. | 在化合物CaCl2中,两个氯离子之间也存在离子键 | |
| D. | 含有离子键的化合物一定是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
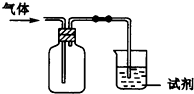 如图装置可用于收集气体X并验证其某些化学性质,你认为不正确的是( )
如图装置可用于收集气体X并验证其某些化学性质,你认为不正确的是( )| 选项 | 气体 | 试剂 | 现象 | 结论 |
| ① | SO2 | 酸性高锰酸钾溶液 | 溶液褪色 | SO2有漂白性 |
| ② | NH3 | 滴有紫色石蕊的盐酸 | 溶液变蓝 | 氨水显碱性 |
| ③ | CO2 | 氯化钡溶液 | 溶液变浑浊 | 碳酸钡难溶于水 |
| ④ | Cl2 | 紫色石蕊试液 | 溶液先变红后褪色 | Cl2有酸性和漂白性 |
| A. | ③④ | B. | ②④ | C. | ①② | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| O═O(g) | H-H(g) | H-O(g) | |
| 1mol化学键断裂时需要吸收的能量/kJ | 496 | X | 463 |
| A. | 920 | B. | 557 | C. | 436 | D. | 188 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com