
【题目】下列分子中,各分子的空间构型、中心原子的杂化方式以及孤电子对数均正确的是
选项 | 分子 | 空间构型 | 杂化方式 | 孤电子对数 |
A | NH3 | 平面三角形 | sp3杂化 | N含有一对孤电子对 |
B | CCl4 | 正四面体 | sp3杂化 | C不含有孤电子对 |
C | H2O | V形 | sp2杂化 | O含有两对孤电子对 |
D | CO32- | 三角锥形 | sp3杂化 | C含有一对孤电子对 |
A. AB. BC. CD. D
【答案】B
【解析】
根据价层电子对互斥理论确定分子空间构型及中心原子杂化方式,价层电子对数=配原子个数+孤电子对数。
A. NH3中心原子的价层电子对数=3+![]() (5-3×1)=4,N原子的杂化方式为sp3,含有一对孤电子对,分子的立体构型为三角锥形,A项错误;
(5-3×1)=4,N原子的杂化方式为sp3,含有一对孤电子对,分子的立体构型为三角锥形,A项错误;
B. CCl4中心原子的价层电子对数=4+![]() (4-4×1)=4,C原子的杂化方式为sp3,没有孤电子对,分子的立体构型为正四面体,B项正确;
(4-4×1)=4,C原子的杂化方式为sp3,没有孤电子对,分子的立体构型为正四面体,B项正确;
C. H2O中心原子的价层电子对数=2+![]() (6-2×1)=4,O原子的杂化方式为sp3,含有两对孤电子对,分子的立体构型为V形,C项错误;
(6-2×1)=4,O原子的杂化方式为sp3,含有两对孤电子对,分子的立体构型为V形,C项错误;
D. CO32- 中心原子的价层电子对数=3+![]() (4+2-3×2)=3,C原子的杂化方式为sp2,没有孤电子对,分子的立体构型为平面三角形,D项错误;
(4+2-3×2)=3,C原子的杂化方式为sp2,没有孤电子对,分子的立体构型为平面三角形,D项错误;
答案选B。


 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案科目:高中化学 来源: 题型:
【题目】有两种新型的应用于液晶和医药的材料W和Z,可用以下路线合成。
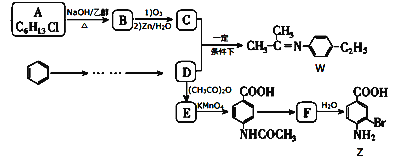
已知以下信息:
① (R1、R2、R3、R4为氢原子或烷烃基)
(R1、R2、R3、R4为氢原子或烷烃基)
②1molB经上述反应可生成2molC,且C不能发生银镜反应
③![]() (易被氧化)
(易被氧化)
④![]() +CH3-CH=CH2
+CH3-CH=CH2 ![]()
请回答下列问题:
(1)化合物A的结构简式____________,A→B的反应类型为_______________。
(2)下列有关说法正确的是____________(填字母)。
A.化合物B中所有碳原子不在同一个平面上
B.化合物W的分子式为C11H16N
C.化合物Z的合成过程中,D→E步骤为了保护氨基
D.1mol的F最多可以和4 molH2反应
(3)C+D→W的化学方程式是________________________。
(4)写出同时符合下列条件的Z的所有同分异构体的结构简式:_____________________。
①遇FeCl3溶液显紫色;
②红外光谱检测表明分子中含有![]() 结构;
结构;
③1H-NMR谱显示分子中含有苯环,且苯环上有两种不同化学环境的氢原子。
(5)设计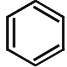 →D合成路线(用流程图表示,乙烯原料必用,其它无机过剂及溶剂任选)______________。
→D合成路线(用流程图表示,乙烯原料必用,其它无机过剂及溶剂任选)______________。
示例:CH3CHO ![]() CH3COOH
CH3COOH ![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】玫瑰的香味物质中包含苧烯,苧烯的键线式为:![]() 。
。
(1)1 mol苧烯最多可以跟________mol H2发生反应。
(2)写出苧烯跟等物质的量的Br2发生加成反应所得产物的可能的结构______________(用键线式表示)。
(3)有机物A是苧烯的同分异构体,分子中含有“![]() ”结构,A可能的结构为_______________(用键线式表示)。
”结构,A可能的结构为_______________(用键线式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
利用甲烷与氯气发生取代反应的副产品生产盐酸的设想在工业上已成为现实。某化学兴趣小组拟在实验室中模拟上述过程,所设计的装置如下图所示:
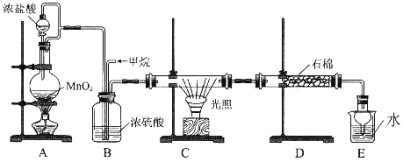
(1)最简单烷烃的空间结构为_______________。
(2)写出装置C中生成一氯甲烷的化学方程式:__________,该反应类型为:_________。
(3)D中石棉上吸附着潮湿的KI粉末,其作用是_________________________。
(4)若题目中甲烷与氯气的体积之比为1∶1,两者反应则得到的产物有____种,其中常温下为气态的有机产物的化学式为:________。
(5)将0.4molCH4与Cl2发生取代,测得4种有机取代物的物质的量相等,则消耗的氯气的物质的量是______________。
(6)烃A为甲烷的同系物,A中有12个氢原子,写出A的同分异构体中,含4个-CH3的结构简式: _________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学--选修5:有机化学基础]
氰基丙烯酸酯在碱性条件下能快速聚合为 ,从而具有胶黏性,某种氰基丙烯酸酯(G)的合成路线如下:
,从而具有胶黏性,某种氰基丙烯酸酯(G)的合成路线如下:

已知:
①A的相对分子量为58,氧元素质量分数为0.276,核磁共振氢谱显示为单峰
②
回答下列问题:
(1)A的化学名称为_______。
(2)B的结构简式为______,其核磁共振氢谱显示为______组峰,峰面积比为______。
(3)由C生成D的反应类型为________。
(4)由D生成E的化学方程式为___________。
(5)G中的官能团有___、 ____ 、_____。(填官能团名称)
(6)G的同分异构体中,与G具有相同官能团且能发生银镜反应的共有_____种。(不含立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释工业生产或应用的化学用语中,不正确的是( )
A. FeCl3溶液刻蚀铜电路板:2Fe3+ + Cu==2Fe2++ Cu2+
B. 向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3·H2O== Al(OH)3↓ + 3NH4 +
C. 将少量二氧化碳通入次氯酸钠溶液中:CO2+H2O+2ClO-== CO32-+2HClO
D. Na2CO3溶液处理水垢:CaSO4(s)+CO32(aq)![]() CaCO3(s)+SO42(aq)
CaCO3(s)+SO42(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】太阳能电池的发展已经进入了第三代。第一代为单晶硅太阳能电池,第二代为多晶硅、非晶硅等太阳能电池,第三代就是铜铟镓硒CIGS(CIS中掺入Ga)等化合物薄膜太阳能电池以及薄膜Si系太阳能电池。镓元素处于同一主族的硼元素具有缺电子性,其化合物往往具有加合性,因而硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-而体现一元弱酸的性质。不考虑空间构型,[B(OH)4]-的结构可用示意图表示为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在溶液中加入过量Na2O2后仍能大量共存的是
A.NH![]() 、Ba2+、Cl-、NO
、Ba2+、Cl-、NO![]() B.K+、SiO
B.K+、SiO![]() 、AlO
、AlO![]() 、SO
、SO![]()
C.Fe2+、Mg2+、SCN-、Cl-D.Na+、SO![]() 、I-、HCO
、I-、HCO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、晶体硅(熔点1410℃)是良好的半导体材料,由粗硅制纯硅过程如下:
![]()
在上述由SiCl4制纯硅的反应中,测得每生成1.12 kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:_________。
Ⅱ、目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,进行如下实验,在体积为1L的密闭容器中,充入1mol CO2和3.25 mol H2,在一定条件下发生反应,测定CO2、CH3OH(g)和H2O(g)的浓度随时间变化如下图所示:
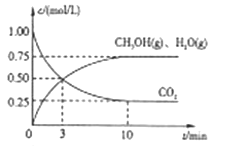
(1)从反应开始到平衡,氢气的平均反应速率υ(H2)=__________ 。
(2)该条件下CO2的转化率为_______。
Ⅲ、下图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:

(1)M极的电极材料为 ___________________。
(2)加入乙醇的铂电极的电极反应式为___________。
(3)在此过程中乙池中某一电极析出金属银4.32g时,此时乙池溶液的体积为400mL,则乙池中溶液的pH为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com