
����Ŀ����������(C12O)�Ǵ�����������������Ȼ����䲿���������£�
�������� | ��ѧ���� |
�����£�C12O���ػ�ɫ�̼������塣 �۵㣺��120.6�棻�е�2.0�� | C12O���ȶ��Ӵ�һ���л����ױ�ը����������ˮ��ͬʱ��Ӧ���ɴ����ᡣ |
ʵ�����Ʊ�ԭ��2Na2CO3+H2O+2Cl2![]() 2NaCl +2NaHCO3+ C12O�� ��������װ�����ʵ���Ʊ�����C12O����̽��������ʵ����ʡ�
2NaCl +2NaHCO3+ C12O�� ��������װ�����ʵ���Ʊ�����C12O����̽��������ʵ����ʡ�

(1)װ��A������X������Ϊ___________��
(2)�����������������װ������˳����A��___________(ÿ��װ������һ��)��
(3)װ��F��ʢװ�Լ�������Ϊ___________��
(4)A�з�Ӧ�����ӷ���ʽΪ___________��
(5)��D���ռ�����Һ̬����ʱֹͣ��Ӧ����Ƽ�ʵ��֤��B�в��������к���NaHCO3��___________��
(6)ʵ����ɺ�ȡE���ձ�����Һ�μ�Ʒ����Һ������Һ��ɫ���ÿ��������ʵ��̽����Һ��ɫ��ԭ��
��� | 0.1mol/LNaClO��Һ/mL | 0.1mol/LNaCl��Һ/mL | 0.1mol/LNaOH��Һ/mL | H2O/mL | Ʒ����Һ | ���� |
I | 5.0 | 0 | 0 | 5.0 | 3�� | �Ͽ���ɫ |
II | 0 | 5.0 | a | 0 | 3�� | ����ɫ |
III | 5.0 | 0 | 0 | 3�� | ������ɫ |
��a=___________��
��������ʵ��ó��Ľ�����___________��
���𰸡���Һ©�� FBCDE ����ʳ��ˮ MnO2+4H++2Cl-![]() Mn2++Cl2��+2H2O ȡB�й����������Թ��У�������ˮ�ܽ⣬�μӹ���BaCl2��Һ�����ã�ȡ�ϲ���Һ����һ�Թ��У��ٵμ�Ba(OH)2��Һ���а�ɫ�������� 5.0 ������������ͬʱ����Һ�ļ���Խǿ������������ҺƯ������Խ����
Mn2++Cl2��+2H2O ȡB�й����������Թ��У�������ˮ�ܽ⣬�μӹ���BaCl2��Һ�����ã�ȡ�ϲ���Һ����һ�Թ��У��ٵμ�Ba(OH)2��Һ���а�ɫ�������� 5.0 ������������ͬʱ����Һ�ļ���Խǿ������������ҺƯ������Խ����
��������
(1)����װ��ͼ��֪װ��A������X������Ϊ��Һ©����
(2)ͨ��Aװ����ȡCl2������Ũ������лӷ��ԣ���ȡ��Cl2�к���HCl���ʣ�Ϊ��ֹ�����Cl2O����ȡ��Ҫ��ͨ��Fװ�ó�ȥHCl���ʣ���ͨ��Bװ�÷�����Ӧ2Na2CO3+H2O+2Cl2![]() 2NaCl +2NaHCO3+C12O����ȡ�õ�C12O������������ˮ��ͬʱ��ˮ��Ӧ���ɴ����ᣬ�����ռ�֮ǰҪ��ͨ��Cװ�ø����ͨ��Dװ���ռ�Cl2O����֤��е�ͣ�����Һ�����ص㣬ͬʱ����Cl2��C12O�������������Ⱦ���������Ҫ��Eװ�ý���β���������ʰ����������������װ������˳����AFBCDE��
2NaCl +2NaHCO3+C12O����ȡ�õ�C12O������������ˮ��ͬʱ��ˮ��Ӧ���ɴ����ᣬ�����ռ�֮ǰҪ��ͨ��Cװ�ø����ͨ��Dװ���ռ�Cl2O����֤��е�ͣ�����Һ�����ص㣬ͬʱ����Cl2��C12O�������������Ⱦ���������Ҫ��Eװ�ý���β���������ʰ����������������װ������˳����AFBCDE��
(3)װ��F�dz�ȥCl2�е�����HCl����ģ�Ϊ����Cl2���ܽ����ģ�Ҫͨ��ʢ�б���ʳ��ˮ����Һ����ȥHCl���ʣ���װ��F��ʢװ�Լ�������Ϊ����ʳ��ˮ��
(4)A��Ũ������MnO2��ϼ�����ȡCl2����Ӧ�����ӷ���ʽΪMnO2+4H++2Cl-![]() Mn2++Cl2��+2H2O��
Mn2++Cl2��+2H2O��
(5)��װ��B��Na2CO3��Cl2��Ӧ��ȡCl2O������Ҫ֤��B�в��������к���NaHCO3����Ҫ�ȼ��������BaCl2��Һ�����ã�ʹ���ܴ��ڵ�Na2CO3ת��ΪBaCO3������ȥ��Ȼ��ȡ�ϲ���Һ����һ�Թ��У��ٵμ�Ba(OH)2��Һ�����а�ɫ�������ɣ�֤��������Ӧ��2NaHCO3+Ba(OH)2=BaCO3��+Na2CO3+2H2O��������̼�ᱵ�������Ӷ���֤������NaHCO3��
(6)��Ҫ��֤ÿ��ʵ��ʱ��Һ���������10mL������a=5.0��
��������ʵ����Կ�������������������ʱ����Һ�ļ���Խ��������������Һ��Ư����Խǿ����Һ�ļ���Խǿ������������ҺƯ������Խ����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��װ�úͷ���������Ӧʵ�飬�ܴﵽʵ��Ŀ�ĵ���
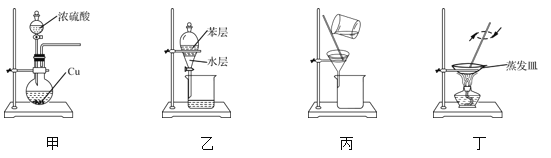
A. ��װ�ü��Ʊ�SO2
B. ��װ���Ҵӵ�ˮ��Һ����ȡ��
C. ��װ�ñ���ȥ������Һ�л��е�KCl����
D. ��װ�ö�������Һ���(NH4)2CO3����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I.������(CH3OCH3)����Ϊ21���͵�����ȼ�ϣ���ҵ����CO��H2Ϊԭ�����������ѡ���֪��
��CO(g)+2H2(g)![]() CH3OH(g) ��H=��99kJ/mol
CH3OH(g) ��H=��99kJ/mol
��2CH3OH(g)![]() CH3OCH3(g)+H2O(g) ��H=��24 kJ/mol
CH3OCH3(g)+H2O(g) ��H=��24 kJ/mol
��CO(g)+H2O(g)![]() H2(g)+CO2(g) ��H=��41 kJ/mol
H2(g)+CO2(g) ��H=��41 kJ/mol
(1)��Ӧ4H2(g)+2CO(g)![]() CH3OCH3(g)+H2O(g)����H=___________��
CH3OCH3(g)+H2O(g)����H=___________��
(2)ij�¶��£���4.0molH2��4.0molCO�����ݻ�Ϊ1L���ܱ������У�������Ӧ3CO(g)+3H2(g)![]() CH3OCH3(g)+CO2(g)��5minʱCO2�����ʵ���Ũ��Ϊ0.5mo1/L��10min��Ӧ�ﵽƽ��״̬����ö����ѵ��������Ϊ25%��
CH3OCH3(g)+CO2(g)��5minʱCO2�����ʵ���Ũ��Ϊ0.5mo1/L��10min��Ӧ�ﵽƽ��״̬����ö����ѵ��������Ϊ25%��
��5minʱCO��ת����=___________��
�����¶��´˷�Ӧ��ƽ�ⳣ��K=___________��
�����д�ʩ����� CH3OCH3ƽ����ʵ���___________(����)��
A.����� CH3OCH3 B.�����¶� C.����ѹǿ D.���ø�Ч����
��.Һ����һ�����õĴ�������
��֪��2NH3(g)![]() N2(g)+3H2(g) ��H=+92.4 kJ/mol
N2(g)+3H2(g) ��H=+92.4 kJ/mol
����������ͬʱ����Ӧ�ڲ�ͬ�������������½�����ͬʱ�����ת����[a(NH3)]�淴Ӧ�¶ȵı仯�����ͼ��ʾ��

(1)��___________������ʱ�������ֽⷴӦ�Ļ�����
(2)a����������״̬___________(������������������)ƽ��״̬��
(3)c��ʱNH3��ת���ʸ���b��ʱNH3��ת���ʣ�ԭ����______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֮�乲��һ��̼ԭ�ӵĻ������Ϊ�ݻ������1��4-��������[2.2]����Ľṹ��ʽΪ![]() ������˵����ȷ����
������˵����ȷ����
A. 1mol���л�����ȫȼ����Ҫ4molO2
B. ���л����� HCOOCH=CH2��Ϊͬ���칹��
C. ���л���Ķ��ȴ�����3��
D. ���л�������ԭ�Ӿ�����ͬһƽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������ɴ�����Ⱦ����Ҫ���ʡ��о���������ķ�Ӧ������������������Ⱦ����Ҫ���塣�ش��������⣺
(1)��֪��2NO2(g)= N2O4(g) ��H=��55.3kJ/mol
N2O5(g)=2NO2(g)+![]() O2(g) ��H=+53.1 kJ/mol
O2(g) ��H=+53.1 kJ/mol
��N2O5(g)=N2O4(g)+![]() O2(g) ��H=___________ kJ/mol
O2(g) ��H=___________ kJ/mol
(2)����ϩ(C2H4)��Ϊ��ԭ������(NO)������������ͼ1������Ӧ��n(NO)�Un(O2)=2�U1�����ܷ�Ӧ�Ļ�ѧ����ʽΪ___________�����������¶ȡ�������(����ɸ�д�������������)�Ĺ�ϵ��ͼ2��Ϊ�ﵽ�������Ч����Ӧ���õ�������___________��

(3)T1�¶�ʱ���ݻ�Ϊ2L�ĺ����ܱ������з�����Ӧ��2NO(g)+O2(g)![]() 2NO2(g) ��H<0��ʵ���ã�����=��(NO)����=2��(O2)����=k��c2(NO)��c(O2)������=(NO2) ����=k��c2(NO2)��k����k��Ϊ���ʳ���ֻ���¶�Ӱ�졣��ͬʱ�̲��������n(NO)��n(O2)�����
2NO2(g) ��H<0��ʵ���ã�����=��(NO)����=2��(O2)����=k��c2(NO)��c(O2)������=(NO2) ����=k��c2(NO2)��k����k��Ϊ���ʳ���ֻ���¶�Ӱ�졣��ͬʱ�̲��������n(NO)��n(O2)�����

�ٴ�0��2s�ڸ÷�Ӧ��ƽ��������(NO)=___________mol/(L��s)��
��T1�¶�ʱ��ѧƽ�ⳣ��K=___________ L/mol�� (�������3λ��Ч����)��
�ۻ�ѧƽ�ⳣ��K�����ʳ���k����k������ѧ��ϵ��K=___________�������������¶ȸı�ΪT2ʱ��k��=k������T2___________T1(�>������<����=")��
����֪2NO(g)+O2(g)![]() 2NO2�ķ�Ӧ����Ϊ��
2NO2�ķ�Ӧ����Ϊ��
��һ��NO+NO![]() N2O2 ���ٷ�Ӧ �ڶ���N2O2+O2��2NO2 ����Ӧ
N2O2 ���ٷ�Ӧ �ڶ���N2O2+O2��2NO2 ����Ӧ
����������ȷ����___________(����)��
A. ��(��һ��������Ӧ)< ��(�ڶ����ķ�Ӧ) B.�ܷ�Ӧ�����ɵڶ�������
C.�ڶ����Ļ�ܱȵ�һ���ĸ� D.�ڶ�����N2O2��O2����ײ100%��Ч
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и���ĵ缫���Ϻ͵��Һ���������ԭ��ص��ǣ�������
A. ͭƬ��ʯī����������ҺB. пƬ��ʯī��������ͭ��Һ
C. пƬ��ͭƬ��ϡ����D. ͭƬ����Ƭ����������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NaC1O3��������ȡ�������ȡ��������Ƽ��������εȡ���ԭ��(��Ҫ�ɷ�ΪNaC1)Ϊԭ���Ʊ������ƵĹ����������£�

��֪��Cr2O72-+H2O![]() 2CrO42-+2H+��
2CrO42-+2H+��
�ش��������⣺
(1)��������ˮ���м���NaOH��Na2CO3��Ŀ����___________________��
(2)����ʱ��ʹ�õIJ����������ձ�����������____________��
(3)��pH��6.4��6.8���¶ȣ�40��50���������µ�⣬���������ղ���ֻ��NaC1O3�����ʱ�����IJ���ΪC12����Һ�з����ķ�Ӧ��C12+H2O====HC1O+H++C1-��HC1O![]() H++C1O-��__________��
H++C1O-��__________��
(4)�������¶Ȳ��˹��ߣ���ԭ����_________________________�������Na2Cr2O7���Ե��ڵ��Һ��ȣ�����ȹ�������Һ����Ҫ����__________(����Cr2O72-������CrO42-��)��
(5)Ϊ��������ˮ��NaC1O3�����ʵ���Ũ�Ƚ�������ʵ�飺
I��ȷ��ȡ10��00mL�������ˮ������������3��H2O2��Һ��ֽ��貢��С�
����ȷ��ȡ0.10mol��L-1��(NH4)2Fe(SO4)2����Һ25��00 mL��300mL��ƿ�У���������ϡ���ᡣ
III����I����Һ����������ƿ�У������������10min�����ȳ�ַ�Ӧ����ȴ�����º���10mL0.4mol��L-1MnSO4��Һ��5mL 85��������Һ����c mol��L-1��KMnO4����Һ�ζ�ʣ���Fe2+����Һ��Ϊ��ɫ�����ζ��յ㣬��ʱ���ĸ������V mL��
�ٲ���I�м���H2O2��Һ��������______________________��
�ڲ�������C1O3-��Fe2+��ԭΪC1-�����ӷ���ʽΪ________________________��
�۸���ˮ��NaC1O3�����ʵ���Ũ��Ϊ________mol��L-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ϡ���ᡢ����ʯ��ˮ���Ȼ�ͭ��Һ�dz��л�ѧ�г��������ʣ��������ʼ�ķ�Ӧ��ϵ��ͼ��ʾ��ͼ����Բ�ཻ����(A��B��C��D)��ʾ���ʼ�ķ�Ӧ�����ж�Ӧ�ĸ���Ӧ���͵�˵����ȷ����

A. ���ֽⷴӦ�����ֽⷴӦ�����Ϸ�Ӧ���û���Ӧ
B. �кͷ�Ӧ���û���Ӧ�����ֽⷴӦ���û���Ӧ
C. ���ֽⷴӦ�����ֽⷴӦ���û���Ӧ���û���Ӧ
D. �ֽⷴӦ�����ֽⷴӦ���û���Ӧ���û���Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л�����ϩ������ȥ��ϩ�õ������ļ��飬������ͨ��ʢ��������һ���Լ���ϴ��ƿ�� ��
A������ʯ��ˮ��ŨH2SO4
B������KMnO4��Һ��ŨH2SO4
C����ˮ��ŨH2SO4
D��ŨH2SO4��NaOH��Һ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com