
已知:硼镁矿主要成分为Mg2B2O5·H2O,硼砂的化学式为Na2B4O7·10H2O。利用硼镁矿制取金属镁及粗硼的工艺流程为:
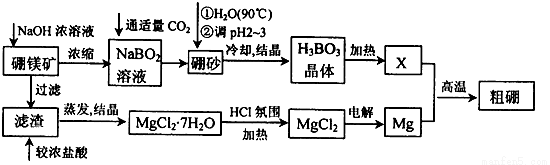
回答下列有关问题:
(1)硼砂中B的化合价为 ,将硼砂溶于热水后,常用稀H2SO4调pH=2~3制取H3BO3,该反应的离子方程式为 。
(2)MgCl2·7H2O需要在HCl氛围中加热,其目的是 。若用惰性电极电解MgCl2溶液,其阴极反应式为 。
(3)镁-H2O2酸性燃料电池的反应原理为 Mg+H2O2+2H+===Mg2++2H2O, 则正极反应式为 。常温下,若起始电解质溶液pH=1,则pH=2时,溶液中Mg2+浓度为______。当溶液pH=6时, (填“有”或“没有”)Mg(OH)2沉淀析出(已知Ksp[Mg(OH)2]=5.6×10-12)。
(4)制得的粗硼在一定条件下生成BI3,BI3加热分解可以得到纯净的单质硼。现将0.020 g粗硼制成的BI3完全分解,生成的I2用0.30 mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液18.00 mL。该粗硼样品的纯度为____(提示:I2+2S2O===2I-+S4O)(结果保留一位小数)。
科目:高中化学 来源:2016届福建省高三上学期12月月考化学试卷(解析版) 题型:选择题
在催化剂、400℃时可实现氯的循环利用,如图是其能量关系图,下列分析正确的是
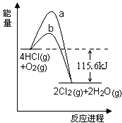
A.曲线a是使用了催化剂的能量变化曲线
B.反应物的总键能高于生成物的总键能
C.反应的热化学方程式为:
4HCl(g)+O2(g) 2Cl2+2H2O(g)﹣115.6 kJ
2Cl2+2H2O(g)﹣115.6 kJ
D.若反应生成2mol液态水,放出的热量高于115.6kJ
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期第四次月考化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.用MgCl2·6H2O制取无水MgCl2时需在HCl气流中进行
B.高锰酸钾溶液可用碱式滴定管盛装
C.Al Cl3溶液蒸干可得到Al Cl3固体
D.碳酸钠溶液的试剂瓶不能是玻璃瓶,可以用玻璃塞
查看答案和解析>>
科目:高中化学 来源:2016届河南省洛阳市高三上学期12月统考化学试卷(解析版) 题型:选择题
红曲素是一种食品着色剂的主要成分,其结构简式如图所示。下列有关红曲素的说法正确的是
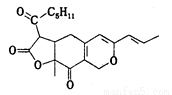
A.红曲素含有两种含氧官能团
B.红曲素分子式为C21H25O5
C.红曲素能使酸性高锰酸钾溶液褪色
D.lmol红曲素最多能与2 mol NaOH反应
查看答案和解析>>
科目:高中化学 来源:2016届河南省洛阳市高三上学期12月统考化学试卷(解析版) 题型:选择题
下列过程中,没有明显实验现象的是
A.向Fe(NO3)2溶液中滴加稀硫酸
B.将HCl通入NaAlO2溶液中
C.加热溶有SO2的品红溶液
D、向碳酸氢钠溶液中滴加氢氧化钠溶液
查看答案和解析>>
科目:高中化学 来源:2016届河南省三门峡市高三上学期第二次精英对抗赛化学试卷(解析版) 题型:选择题
电子层数相同的短周期元素X、Y、Z、W,其中X的最外层电子数比K层少1,Y的最外层电子数比K层多l,Z的单质是一种半导体材料,常用于制造太阳能电池,W的原子半径是同周期中最小的。下列推断中正确的是
A.Z的氢化物的热稳定性强于W的氢化物
B.Z的氧化物与水反应可制得相应的含氧酸
C.X、Y、W的原子半径依次减小,对应的离子半径依次增大
D.X、Y、W的最高价氧化物对应水化物之间互相都能发生反应
查看答案和解析>>
科目:高中化学 来源:2016届河南省三门峡市高三上学期第二次精英对抗赛化学试卷(解析版) 题型:选择题
下列叙述不正确的是
A、钢铁水闸可用牺牲阳极或外加电流的阴极保护法防止其生腐蚀
B、反应SO2(g)+2H2S(g)=3S(S)+2H2O(l)在常温下能自发进行,则该反应的△H<0
C、0.1mol·L-1的CH3COOH溶液加水稀释,溶液的pH和溶液中水的电离程度均增大
D、常温下,将等体积、等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得溶液pH<7,存在KW/c(H+)>1.0×10-7 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期12月月考化学试卷(解析版) 题型:填空题
高铁酸钾是一种重要的绿色净水剂,具有净水和消毒双重功能。某课外学习小组设计如下方案制备高铁酸钾:
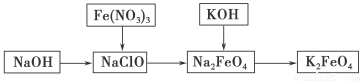
(1)高铁酸钾中铁元素的化合价为________,推测它具有的化学性质是__________________。
(2) 已知Fe2O3与KNO3和KOH的混合物加热共融也可制得高铁酸钾。完成并配平下列化学方程式:

(3)将KOH加入含Na2FeO4的溶液中搅拌半小时,静置,过滤粗产品,该过程发生的反应为2KOH+Na2FeO4===K2FeO4+2NaOH,根据复分解反应原理,高铁酸钠的溶解度________(填“大于”、“小于”或“等于”)高铁酸钾的溶解度。
(4)为测定含铁溶液中铁元素的总含量,实验操作:
①准确量取20.00mL含铁溶液于带塞锥形瓶中,加入足量H2O2,待充分反应后,加热除去过量H2O2;
②加入过量KI充分反应后,再用0.1000 mol·L-1 Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00 ml。已知: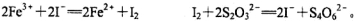
①写出滴定选用的指示剂 ,滴定终点观察到的现象 。
②溶液Ⅰ中铁元素的总含量为 g·L-1。若滴定前溶液中H2O2没有除尽,所测定的铁元素的含量将会 (填“偏高” “偏低” “不变”)。
查看答案和解析>>
科目:高中化学 来源:2016届山东省北校高三上学期第二次单元测试化学试卷(解析版) 题型:选择题
向某恒容密闭容器中充入一定量C02和H2,发生反应: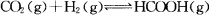 测得平衡体系中C02的百分含量(C02%)与反应温度变化的关系如图所示。下列物理量 中,a点大于b点的是
测得平衡体系中C02的百分含量(C02%)与反应温度变化的关系如图所示。下列物理量 中,a点大于b点的是

①:正反应速率 ②逆反应速率 ③HCOOH(g)的浓度 ④对应温度时的平衡常数
A. ①② B.①③ C.②④ D.③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com