
【题目】工业上以软锰矿(主要成分是MnO2,还含有少量SiO2、Fe2O3)为主要原料制备高性能的磁性材料碳酸猛(MnCO3)。其工业流程如图所示,下列说法错误的是
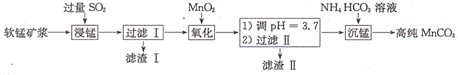
A.滤渣I可用于制造光导纤维、滤渣II可用于制作颜料
B.“浸锰”过程MnO2参与反应的化学方程式为MnO2十SO2=MnSO4
C.“沉锰”时,反应体系的温度越高,越有利于生成MnCO3
D.检验高纯碳酸锰是否洗涤干净,可选用BaCl2溶液和盐酸试剂
【答案】C
【解析】
A.分析流程可知,滤渣I为二氧化硅,可用于制造光导纤维、滤渣II为氢氧化铁,氢氧化铁受热分解生成三氧化二铁,三氧化二铁可用于制作颜料,A正确;
B.软锰矿浆中通入足量的二氧化硫,二氧化锰与二氧化硫发生氧化还原反应生成硫酸锰,反应方程式为MnO2十SO2=MnSO4,B正确;
C.“沉锰”时,反应体系的温度越高,碳酸氢铵越容易分解,碳酸氢铵的原料利用率越低,C错误;
D.生成的碳酸锰沉淀需经充分洗涤,若未洗涤干净,洗涤液中含有硫酸根离子,故检验洗涤液中是否含有硫酸根离子即可,方法为:取1~2mL最后一次洗涤液与试管中,滴加盐酸酸化,无明显现象,在滴加氯化钡溶液,若无白色沉淀产生,则洗涤干净,D正确;
答案选C。


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:
【题目】2V L Fe2(SO4)3溶液中含有a g SO42—,取此溶液V L,用水稀释至2V L,则稀释后溶液中Fe3+的物质的量浓度为
A.![]() mol·L-1B.
mol·L-1B.![]() mol·L-1C.
mol·L-1C.![]() mol·L-1D.
mol·L-1D.![]() mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】nL三种气态烃混合物与足量氧气混合点燃后,恢复到原来状态(常温常压),体积共缩小2nL,这三种烃不可能的组合是( )
A. CH4、C2H4、C3H4以任意比混合
B. C3H8、C4H8、C2H2以11:14:26的质量之比混合
C. CH4、C2H2、C3H6以1:2:2的体积比混合
D. C2H6、C4H6、C2H2以2:1:2的物质的量之比混合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下为配制250 mL 0.2 mol·L-1 Na2CO3溶液的示意图。
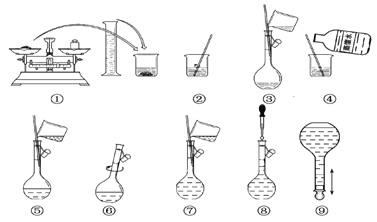
回答下列问题:
(1)在容量瓶的使用方法中,下列操作不正确的是________。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近标线1~2 cm处,用滴管滴加蒸馏水到标线
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近标线1~2 cm处,用滴管滴加蒸馏水到标线
E.盖好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转并摇动多次
(2)①中称得Na2CO3________g。
(3)玻璃棒在②、③两步中的作用分别是________、________。
(4)若出现如下情况,所配溶液浓度偏低的有:________
A.某同学在第⑧步观察液面时仰视;
B.没有进行操作步骤④和⑤;
C.在第⑤步不慎有少量液体流到容量瓶外;
D.在步骤①中,药品放在右盘,砝码放在左盘(使用游码)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将CH4设计成燃料电池,其利用率更高,装置示意如图(A、B为多孔性碳棒)持续通入甲烷,在标准状况下,消耗甲烷体积VL。则下列说法错误的是( )

A.通入CH4的一端为原电池的负极,通入空气的一端为原电池的正极
B.0<V≤22.4 L时,电池总反应的化学方程式为CH4+2O2+2KOH=K2CO3+3H2O
C.22.4 L<V≤44.8 L时,负极电极反应为CH4-8e-+![]() +3H2O=
+3H2O=![]()
D.V=33.6 L时,溶液中只存在阴离子![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组设计步骤用滴定法测定AgBrO3的溶度积常数.回答下列问题:
步骤I:试剂的配制
分别配制1L0.025molL-1KBrO3溶液、1L0.025rrolL-1AgNO3溶液、lL0.05molL-1Na2S2O3溶液。
(1)配制Na2S2O3溶液所使用的蒸馏水必须经过煮沸、冷却后才能使用,其目的是杀菌、除______________(写名称)及二氧化碳。
步骤II:AgBrO3饱和溶液配制
用棕色滴定管量取20.00mL0.025molL-1AgNO3溶液于干燥的锥形瓶中,然后用另一支滴定管量取20.00mL0.025molL-1KBrO3溶液注入到锥形瓶中,摇动锥形瓶使沉淀完全,把沉淀陈化3~5min,用过滤器过滤,滤液用于燥洁净的小烧杯盛接。
(2)量取AgNO3溶液所使用的滴定管为棕色的目的是______________。
(3)如果滤液浑浊需要进行的操作为______________。
步骤III:AgBrO3饱和溶液中BrO3-浓度的测定
准确量取20.00mL所得滤液注入碘量瓶中,再加入20mL10%的KI溶液、l5mLlmolL-1的硫酸并加50.00rnL水混匀,放置3~5min,以淀粉为指示剂,用Na2S2O3溶液滴定,消耗Na2S2O3溶液17.86mL(发生的反应BrO3-+6H++6I-=Br-+3I2+3H2O;2Na2S2O3+I2=Na2S4O6+2NaI)。
(4)滴定到终点时的现象为______________。
(5)滤液中BrO3-的浓度为______________(保留3位有效数字,下同),AgBrO3的溶度积测定值为______________。
(6)步骤II中滤液若没有澄清,会使测量值______________(填“偏高”“偏低”或“无影响”,下同);盛接滤液的小烧杯中有少量水存在,会使测量值________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硅是一种化工原料,可以制备一系列物质。下列说法正确的是( )
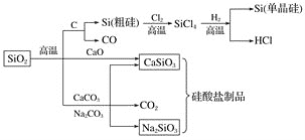
A.图中所有反应都不属于氧化还原反应
B.硅酸盐的化学性质稳定,常用于制造光导纤维
C.可用盐酸除去石英砂(主要成分为SiO2)中少量的碳酸钙
D.普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等。
(1)Fe2+基态核外电子排布式为______。
(2)科学研究表明用TiO2作光催化剂可将废水中CN-转化为OCN-、并最终氧化为N2、CO2。OCN-中三种元素的电负性由大到小的顺序为_______。
(3)与CN-互为等电子体的一种分子为______(填化学式);1mol Fe(CN)63-中含有σ键的数目为______。
(4)铁的另一种配合物Fe(CO)5熔点为-20.5℃,沸点为103℃,易溶于CCl4,据此可以判断Fe(CO)5晶体属于_______(填晶体类型)。
(5)铁铝合金的一种晶体属于面心立方结构,其晶胞可看成由8个小体心立方结构堆砌而成。已知小立方体如图所示。该合金的化学式为_______。
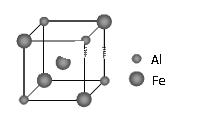
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com