
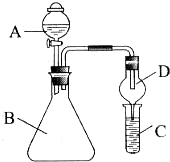
 利用如图装置验证同主族元素非金属性的变化规律.
利用如图装置验证同主族元素非金属性的变化规律.

 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:
| A、摩尔是物质的数量单位,含有6.02×1023个微粒的物质叫做1摩尔 |
| B、1mol氧含有6.02×1023个氧原子 |
| C、在标准状况下,任何物质的摩尔体积约为22.4L/mol |
| D、一定质量的气体的体积随压强增大和温度降低而变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验编号 | c(HA)/mo1?L-1 | c(NaOH)/mo1?L-1 | 反应后溶液pH |
| 甲 | 0.1 | 0.1 | PH=9 |
| 乙 | c1 | 0.2 | PH=7 |
| A、甲反应后的溶液中:c(HA)+c(A-)=0.05mo1?L-1 |
| B、c1一定大于0.2 mo1?L-1 |
| C、0.1 mo1?L-1的HA溶液中由水电离出的c(H+)=1×l0-13mo1/L |
| D、乙反应后的溶液中:c(Na+)<c(HA)+c(A-) |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 1 |
| 2 |
| 3 |
| 2 |
| N | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 铝是地壳中含量最高的金属元素,在所有的元素中位居第三位.
铝是地壳中含量最高的金属元素,在所有的元素中位居第三位.- 4 |
- 4 |
| I1 | I2 | I3 | I4 | … |
| 496 | 4562 | 6912 | 9540 | … |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com