
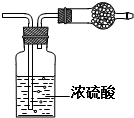
 某无色气体可能由O2、CO、CO2、HCl、NH3、NO、Br2中的一种或几种组成,通过图中洗气瓶后气体体积减少(该装置前后都不与大气直接相连),通过干燥管(内盛放Na2O2)后气体呈红棕色,则下列推断正确的是( )
某无色气体可能由O2、CO、CO2、HCl、NH3、NO、Br2中的一种或几种组成,通过图中洗气瓶后气体体积减少(该装置前后都不与大气直接相连),通过干燥管(内盛放Na2O2)后气体呈红棕色,则下列推断正确的是( )| A、原气体中一定有NO和O2 |
| B、原气体中一定有NH3、NO、CO2、CO |
| C、原气体中一定没有CO |
| D、原气体中一定没有HCl、Br2、O2 |


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 两种有机物A、B的分子式均为C11H12O5,均能发生如图变化.
两种有机物A、B的分子式均为C11H12O5,均能发生如图变化.查看答案和解析>>
科目:高中化学 来源: 题型:
 已知:①H2O(g)═H2O(l)△H2=-44kJ?mol-1
已知:①H2O(g)═H2O(l)△H2=-44kJ?mol-1| A、反应②中的能量变化如图所示,则△H2=E1-E3 |
| B、H2的燃烧热为△H=-241.8kJ?mol-1 |
| C、由反应③知在温度一定的条件下,在一恒容密闭容器中通入1molN2和3molH2,反应后放出的热量为92.4kJ |
| D、反应③中加入催化剂,通过降低反应所需的活化能来增大反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
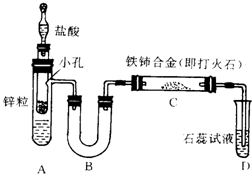 已知亚硝酸铵很不稳定,在溶液中加热能分解生成氮气和水.有人设计以下装置(A中盛有饱和NaNO2与NH4Cl的混合溶液)来进行有关实验.
已知亚硝酸铵很不稳定,在溶液中加热能分解生成氮气和水.有人设计以下装置(A中盛有饱和NaNO2与NH4Cl的混合溶液)来进行有关实验.查看答案和解析>>
科目:高中化学 来源: 题型:
| n |
| 2 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com