
����Ŀ����NA���������ӵ���������ֵ��������Ȼ�ѧ����ʽC2H2(g)��![]() O2(g)===2CO2(g)��H2O(l)����H����1300 kJ��mol��1��˵���У���ȷ������ ��
O2(g)===2CO2(g)��H2O(l)����H����1300 kJ��mol��1��˵���У���ȷ������ ��
A. ת��10NA������ʱ���÷�Ӧ�ų�1300 kJ������
B. ����NA��Һ̬ˮ����ʱ������1300 kJ������
C. ��2NA��̼�����õ��Ӷ�����ʱ���ų�1300 kJ������
D. ��10NA��̼�����õ��Ӷ�����ʱ���ų�1300 kJ������

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������½������г���0.8molSO2, 0.2molO2, 0.6molSO3���Ϊ2L���ܱ������У�������Ӧ��2SO2 (g)+ O2 (g)2SO3(g),�ﵽ��ѧ��Ӧ��ʱ��SO3���ʵ��������ǣ��� ��mol
A. 0B. 0.3C. 1.0D. 1.5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�Ȼ�ѧ����ʽ��SO2(g)+ 1/2O2(g) ![]() SO3(g) ��H���D98.32kJ��mol���������г���2molSO2��1molO2��ַ�Ӧ�����շų�������Ϊ�� ��
SO3(g) ��H���D98.32kJ��mol���������г���2molSO2��1molO2��ַ�Ӧ�����շų�������Ϊ�� ��
A. 196.64kJB. ��98.32kJ
C. ��196.64kJD. ����196.64kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��COCl2(g)![]() CO(g)��Cl2(g)����H��0������Ӧ�ﵽƽ��ʱ�����д�ʩ�������¡��ں���ͨ��ϡ�����塡������COŨ�ȡ��ܼ�ѹ���ݼӴ�������ѹͨ��ϡ�����壬�����COCl2ת���ʵ���(����)
CO(g)��Cl2(g)����H��0������Ӧ�ﵽƽ��ʱ�����д�ʩ�������¡��ں���ͨ��ϡ�����塡������COŨ�ȡ��ܼ�ѹ���ݼӴ�������ѹͨ��ϡ�����壬�����COCl2ת���ʵ���(����)
A. �٢ڢ� B. �٢ܢ� C. �ڢۢ� D. �ۢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����Ȼ�ѧ����ʽ��
�� H2(g)+![]() O2(g)��H2O(l) ��H ���D285kJ/mol
O2(g)��H2O(l) ��H ���D285kJ/mol
�� H2(g)+![]() O2(g)��H2O(g) ��H ���D241.8kJ/mol
O2(g)��H2O(g) ��H ���D241.8kJ/mol
�� C(s)+![]() O2(g)��CO(g) ��H ���D110.4 kJ/mol
O2(g)��CO(g) ��H ���D110.4 kJ/mol
�� C(s)+ O2(g)��CO2(g) ��H ���D393.5 kJ/mol
�ش����и��ʣ�
��1��������Ӧ�����ڷ��ȷ�Ӧ����___________��
��2��C��ȼ����Ϊ_________________��
��3��ȼ��10g H2����Һ̬ˮ���ų�������Ϊ_____________________��
��4��COȼ�յ��Ȼ�ѧ����ʽΪ______________________��
��5��Ϊ�˿�������ЧӦ��������ѧ������˲������롣���˸���Һ̬CO2�ܶȴ��ں�ˮ�ܶȵ���ʵ�����뽫CO2Һ������������ף��Լ��ٴ����е�CO2��ΪʹCO2Һ�����ɲ�ȡ�Ĵ�ʩ________��
a ��ѹ�����¡��������������� b ��ѹ������
c ��ѹ�����¡��������������� d ��ѹ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪H2��ȼ����Ϊ��H����285.8 kJ��mol��1��CO��ȼ����Ϊ��H����282.8 kJ��mol��1������H2��CO��ɵĻ������5.6 L(��״��)�������ȼ�պų�������Ϊ71.15 kJ��������Һ̬ˮ������˵����ȷ����
A. COȼ�յ��Ȼ�ѧ����ʽΪ2CO(g)��O2(g)===2CO2(g)����H����282.8 kJ��mol��1
B. H2ȼ�յ��Ȼ�ѧ����ʽΪ2H2(g)��O2(g)===2H2O(g)����H����571.6 kJ��mol��1
C. ȼ��ǰ���������CO���������Ϊ60%
D. ȼ�պ�IJ���ȫ���������Ĺ����������ÿɲ���0.125 mol O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ѿ�298K��101kPaʱ������˵������ȷ����
��Ӧ1��4Fe(s)+3O2(g) = 2Fe2O3 (s) ��H1 ����1648 kJ/mol
��Ӧ2��C(s) + O2 (g) = CO2 (g) ��H2 = ��393 kJ/mol
��Ӧ3��2Fe(s)+2C(s) +3O2(g) = 2FeCO3(s) ��H3 ����1480 kJ/mol
��Ӧ4��2FeCO3(s) +1/2O2(g) =2CO2(g) +Fe2O3(s) ��H4
A. ������Ӧ1.2.3.4������ѧ���Է����ƶ��ܴ�
B. ��Ӧ1��3�ڽϵ��¶������Է���Ӧ����Ӧ4��������Ӧ
C. �Է���Ӧ������Ӧһ���ܷ����������жϹ��̵ķ�������ȷ�����̷���������
D. ��Ӧ1��ʾ����������ȼ�յ��Ȼ�ѧ����ʽ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����( )
A.ͬ��Ԫ�ص��������ض���ͬ
B.��ͬԪ��ԭ�ӵ��������ض���ͬ
C.ԭ�Ӻ˶��������Ӻ����ӹ��ɵ�
D.���Ǻ����������ͬ�����ض�����ͬһԪ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס��ҡ�����������H+��Na+��Al3+��Ba2+��OH-��Cl-��HCO3-�����е�������ɵ���Һ�����Է�����ͼת��������˵����ȷ����
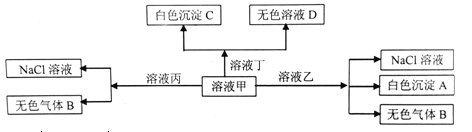
A. ��ΪHCl����ΪNaHCO3
B. ��Һ���л����Դ�������������У�Fe2+��NO3-��SO42-
C. �ڼ��еμӶ���ʼ��Ӧ�����ӷ���ʽ��HCO3-+Ba2++OH-=BaCO3��+H2O
D. ��ɫ����A�����ܽ�����ҺD��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com