
| A. | 用NH3表示反应①的速率为1 mol/(L•min) | |
| B. | 体系中颜色不再变化时,可判断反应均已达平衡 | |
| C. | 该温度下反应①的平衡常数为20 mol2/L2 | |
| D. | 加压时反应②的平衡不会移动 |
分析 反应①的平衡常数k=c(NH3)•c(HI),NH4I分解生成的HI为平衡时HI与分解的HI之和,即为NH4I分解生成的NH3,由反应②可知分解的c(HI)为平衡时c(H2)的2倍,求出为NH4I分解生成的NH3,
A.根据v=$\frac{△c}{△t}$计算出用氨气表示的反应速率;
B.达到平衡状态时,正逆反应速率相等,各组分的浓度不再变化,据此进行判断;
C.代入反应①的平衡常数K=c(NH3)•c(HI)计算;
D.加压时,由于反应①中平衡向着逆向移动,导致体系中HI的浓度减小,则反应②的平衡向着逆向移动.
解答 解:平衡时c(HI)=4mol•L-1,HI分解生成的H2的浓度为0.5mol•L-1,
NH4I分解生成的HI的浓度为:4mol•L-1+2×0.5mol•L-1=5mol•L-1,所以NH4I分解生成的NH3的浓度为5mol•L-1,
A.5min后达平衡时,用氨气表示的反应速率为:v=$\frac{5mol/L}{5min}$=1mol/(L•min),故A正确;
B.体系中只有碘单质有色,则体系中颜色不再变化时,说明该反应的正逆反应速率相等,各组分浓度不再变化,可判断反应均已达平衡,故B正确;
C.所以反应①的平衡常数K=c(NH3)•c(HI)=5mol•L-1×4mol•L-1=20mol2•L-2,故C正确;
D.加压后,反应①向着逆向移动,则体系中HI的浓度减小,反应②向着逆向移动,故D错误;
故选D.
点评 本题考查了化学平衡的影响及计算,题目难度中等,根据反应计算出平衡时氨气的浓度为解答关键,注意掌握化学平衡及其影响因素,明确化学平衡常数、化学反应速率的概念及计算方法.


科目:高中化学 来源: 题型:选择题
| A. | 1.5mol | B. | 1mol | C. | 0mol | D. | 0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂发生皂化反应能生成甘油 | |
| B. | 蛋白质溶液遇醋酸铅溶液发生盐析 | |
| C. | 氨基酸、二肽、蛋白质均既能跟强酸反应又能跟强碱反应 | |
| D. | 乙二醇、甲醛、α-羟基丙酸(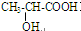 )都可发生缩聚反应 )都可发生缩聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | ① | ② | ③ | 实验结论 | 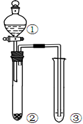 |
| A | 稀硫酸 | Na2CO3 | C6H5ONa | 酸性:H2CO3>C6H5OH | |
| B | 液溴和苯 | 铁屑 | AgNO3溶液 | 液溴和苯发生取代反应 | |
| C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | SO2与可溶性钡盐可以生成白色沉淀 | |
| D | 浓盐酸 | KMnO4 | FeBr2溶液 | 氧化性:Cl2>Br2>Fe3+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 Cr2O72-+H2O,pH小,c(H+)浓度大,平衡正移,使测定结果不准确.
Cr2O72-+H2O,pH小,c(H+)浓度大,平衡正移,使测定结果不准确.| 金属离子 | Ksp | pH(10-1 mol•L-1) | pH(10-5 mol•L-1) |
| Fe3+ | 4.0×10-38 | 2.7 | 3.7 |
| Cr3+ | 6.0×10-31 | 4.3 | 5.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用铜片、铅笔芯作电极插入稀硫酸中 | |
| B. | 用两个铜片作电极插入硝酸银溶液中 | |
| C. | 用锌片、铜片作电极插入番茄中 | |
| D. | 用铜片、铁片作电极插入酒精中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Se>S | B. | 沸点:H2S>H2Se | ||
| C. | 稳定性:H2S>H2Se | D. | 酸性:H2SO4>H2SeO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
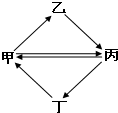 下列各组物质按如图所示转化关系每一步都能一步实现的是
下列各组物质按如图所示转化关系每一步都能一步实现的是| 甲 | 乙 | 丙 | 丁 | |
| A | FeCl3 | FeCl2 | Fe2O3 | Fe(OH)3 |
| B | Cu | CuO | CuSO4 | CuCl2 |
| C | C | CO | CO2 | H2CO3 |
| D | NH3 | NO | NO2 | HNO3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com