
| A. | 1.0 mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) | |
| B. | 1.0 mol/L NH4Cl溶液:c(NH4+)=c(Cl-) | |
| C. | 向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | 1 mol/L CH3COONa溶液,c(CH3COO-)=1 mol/L |
分析 A.根据碳酸钠溶液中的质子守恒分析;
B.氯化铵溶液中,铵根离子部分水解,导致铵根离子浓度减小;
C.该离子浓度关系违反了电荷守恒;
D.醋酸根离子部分水解,醋酸根离子的浓度小于1mol/L.
解答 解:A.根据Na2CO3溶液中的质子守恒可得:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3),故A正确;
B.NH4Cl溶液中,铵根离子部分水解,导致铵根离子部分水解,则c(NH4+)<c(Cl-),故B错误;
C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液,则c(H+)>c(OH-),根据电荷守恒可知:c(CH3COO-)>c(Na+),则正确的离子浓度大小为:c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故C错误;
D.CH3COONa溶液中,醋酸根离子部分水解,导致醋酸根离子的浓度减小,则c(CH3COO-)<1 mol/L,故D错误;
故选A.
点评 本题考查了离子浓度大小比较,题目难度中等,明确盐的水解原理为解答关键,注意掌握电荷守恒、物料守恒的含义及应用方法,试题培养了学生的分析能力及灵活应用能力.


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:解答题

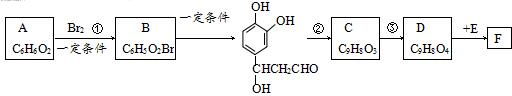
 ;D
;D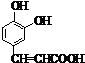 .
.
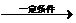
 +nH2O.
+nH2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 探究温度对反应速率影响时,分别水浴加热硫代硫酸钠溶液、硫酸溶液到一定温度,再将两溶液混合 | |
| B. | 用简易量热计测定反应热,使用碎泡沫隔热保温、环形玻璃搅拌棒搅拌、量取达到的最高温度,计算反应热,取2~3 次的实验平均值 | |
| C. | H2O2在过氧化氢酶的催化下,随着温度的升高,分解速率持续加快 | |
| D. | 欲粗略测定某未知浓度的醋酸溶液中醋酸的电离常数Ka,应做的实验和所需的试剂(或试纸)分别为中和滴定实验和pH试纸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 温度越高,K值越大 | B. | K值越大,正反应速率越大 | ||
| C. | K值的大小与起始浓度有关 | D. | K值越大,反应物的转化率越大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑤ | B. | ②④⑤ | C. | ③④⑤ | D. | ②③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硝酸保存在棕色试剂瓶中 | B. | 少量金属钠可保存在煤油里 | ||
| C. | 新制氯水保存在棕色试剂瓶中 | D. | 浓硫酸保存在橡胶塞试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率 | |
| B. | 合成氨工厂通常采用20 Mpa~50 MPa压强,以提高原料的利用率 | |
| C. | 打开啤酒瓶盖后有大量泡沫溢出 | |
| D. | 夏天将食品储藏在冰箱中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com