
| A. | 0.1 mol/L的HCl与0.1 mol/L的NH3•H2O等体积混合,溶液中的c(NH4+)>c(Cl-) | |
| B. | pH=3的HCl与pH=11的氨水等体积混合,溶液中的c(OH-)>c(H+) | |
| C. | pH=11的NaCN溶液中,由水电离出来的c(OH-)=c(H+) | |
| D. | CO2、SO2的水溶液能导电,但它们是非电解质 |
分析 A.0.1 mol/L的HCl与0.1 mol/L的NH3•H2O等体积混合,生成氯化铵溶液,溶液中NH4+离子水解;
B.pH=3的HCl与pH=11的氨水等体积混合,一水合氨存在电离平衡,反应后又电离出氢氧根离子,溶液显碱性;
C.水溶液中水电离出的氢离子和氢氧根离子浓度相同;
D.水溶液中和熔融状态下都不导电的化合物为非电解质.
解答 解:A.0.1 mol/L的HCl与0.1 mol/L的NH3•H2O等体积混合,生成氯化铵溶液,溶液中NH4+离子水解,溶液中的c(NH4+)<c(Cl-),故A错误;
B.pH=3的HCl与pH=11的氨水等体积混合,一水合氨存在电离平衡,反应后又电离出氢氧根离子,溶液显碱性,溶液中的c(OH-)>c(H+),故B正确;
C.pH=11的NaCN溶液中,阴离子水解溶液显碱性,但由水电离出来的c(OH-)=c(H+),故C正确;
D.CO2、SO2的水溶液能导电是生成了碳酸和亚硫酸为电解质,本身不能电离它们是非电解质,故D正确;
故选A.
点评 本题考查了弱电解质电离平衡、溶液酸碱性的判断、盐类水解原理、电解质和非电解质概念等,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 常温下,将pH=3的盐酸和pH=5的硫酸等体积混合,所得溶液的pH=4 | |
| B. | 电解质溶液导电时必将发生氧化还原反应,电解过程是将电能转化为化学能 | |
| C. | 电解氯化镁饱和溶液,可制得金属镁 | |
| D. | 铅蓄电池在放点和充电时电池内硫酸的质量分数均变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2SO2+O2?2SO3△H=-196.6 kJ•mol-1 | |
| B. | H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8 kJ•mol-1 | |
| C. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ | |
| D. | C(s)+O2(g)═CO2(g)△H=393.5 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
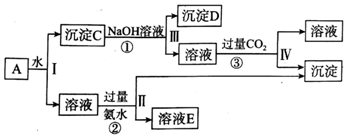
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Z的熔点较低 | B. | Z可表示为M2Y | ||
| C. | M离子和Y离子的核外电子排布相同 | D. | M形成+2价阳离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸馏 | B. | 升华 | C. | 浸取 | D. | 分液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com