

| n |
| V |
| 5.74g |
| 143.5g/mol |
| 0.04mol |
| 0.25L |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.1mol/L Na2CO3��Һ��c��OH-��=c��HCO3-��+c��H+��+2c��H2CO3�� |
| B��0.1mol/L NH4Cl��Һ��c��NH4+����c��Cl-�� |
| C�����������Һ�м����������ᣬ�õ������Ի����Һ��c��Na+����c��CH3COO-����c��H+����c��OH-�� |
| D�����������ʵ���Ũ����Ȣ�NH4HSO4���ڣ�NH4��2SO4���ۣ�NH4��2CO3������Һ��c��NH4+�����٣��ڣ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
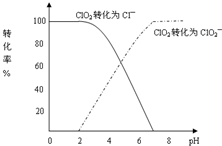 �������ȣ�ClO2����һ����ˮ�����ȷ����й㷺Ӧ�õĸ�Ч��ȫ����������Cl2��ȣ�ClO2�������и�������ɱ�����������Ҳ��������������DZ��Σ�����л��ȴ����ClO2������������ˮ��pHΪ5.5��6.5��������һ���������岻��������������ӣ�ClO2-����2001���ҹ��������涨������ˮ��ClO2-�ĺ���Ӧ������0.2mg?L-1������ˮ��CIO2��CIO2-�ĺ��������������������вⶨ��CIO2��I-��ԭΪCIO2-��Cl-��ת��������ҺpH�Ĺ�ϵ��ͼ��ʾ����pH��2.0ʱ��CIO2-Ҳ�ܱ�I-��ȫ��ԭ��Cl-����Ӧ���ɵ�I2�ñ�Na2S2O3��Һ�ζ���
�������ȣ�ClO2����һ����ˮ�����ȷ����й㷺Ӧ�õĸ�Ч��ȫ����������Cl2��ȣ�ClO2�������и�������ɱ�����������Ҳ��������������DZ��Σ�����л��ȴ����ClO2������������ˮ��pHΪ5.5��6.5��������һ���������岻��������������ӣ�ClO2-����2001���ҹ��������涨������ˮ��ClO2-�ĺ���Ӧ������0.2mg?L-1������ˮ��CIO2��CIO2-�ĺ��������������������вⶨ��CIO2��I-��ԭΪCIO2-��Cl-��ת��������ҺpH�Ĺ�ϵ��ͼ��ʾ����pH��2.0ʱ��CIO2-Ҳ�ܱ�I-��ȫ��ԭ��Cl-����Ӧ���ɵ�I2�ñ�Na2S2O3��Һ�ζ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��950 mL 111.2 g |
| B��500 mL 117.0g |
| C��1000 mL 117.0 g |
| D��1000 mL 111.2 g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
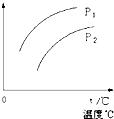 ���ݻ�һ�����ܱ������з������淴ӦY��g��+2X��g��?2Z��g������H��0��ƽ���ƶ���ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
���ݻ�һ�����ܱ������з������淴ӦY��g��+2X��g��?2Z��g������H��0��ƽ���ƶ���ϵ��ͼ��ʾ������˵����ȷ���ǣ�������| A��P1��P2��������ָY���������� |
| B��P1��P2��������ָX��ת���� |
| C��P1��P2��������ָZ���������� |
| D��P1��P2��������ָ��������ƽ��Ħ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��pH=2�������pH=12��NaOH��Һ�������Ϻ���Һ��pH=7 | ||
| B��pH=11�İ�ˮ��c��OH-��=0.1mol?L-1 | ||
C���������еμӰ�ˮ����Һ��pH=6��������Һ��c(Cl-)��c(N
| ||
| D����pH=4.5������ϡ��100������Һ��pH=6.5 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com