
弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。
Ⅰ.已知H2A在水中存在以下平衡:H2A=H++HA-,HA-??H++A2-。
(1)常温下NaHA溶液的pH________(填序号),原因是_________________。
A.大于7 B.小于7
C.等于7? D.无法确定
(2)某温度下,若向0.1 mol·L-1的NaHA溶液中逐滴滴加0.1 mol·L-1KOH溶液至溶液呈中性(忽略混合后溶液的体积变化)。此时该混合溶液中的下列关系一定正确的是________。
A.c(H+)·c(OH-)=1.0×10-14
B.c(Na+)+c(K+)=c(HA-)+2c(A2-)
C.c(Na+)>c(K+)
D.c(Na+)+c(K+)=0.05 mol·L-1
(3)已知常温下H2A的钙盐(CaA)的饱和溶液中存在以下平衡:CaA(s)??Ca2+(aq)+A2-(aq) ΔH>0。若要使该溶液中Ca2+浓度变小,可采取的措施有________。
A.升高温度?????????????????? B.降低温度
C.加入NH4Cl晶体??????????? D.加入Na2A固体
Ⅱ.含有Cr2O72-的废水毒性较大,某工厂废水中含5.0×10-3 mol·L-1的Cr2O72-。为了使废水的排放达标,进行如下处理:
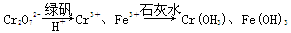
(1)该废水中加入绿矾和H+,发生反应的离子方程式为____________________。
(2)若处理后的废水中残留的c(Fe3+)=2.0×10-13 mol·L-1,则残留的Cr3+的浓度为________。
(已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31)
Ⅰ.(1)B NaHA只能发生电离,不能发生水解
(2)BC
(3)BD
Ⅱ.(1)Cr2O72-+6Fe2++14H+===2Cr3++6Fe3++7H2O
(2)3.0×10-6mol·L-1
【解析】H2A在水中的一级电离进行完全,则HA-不水解只电离,故NaHA溶液呈酸性。HA-在水中部分电离,0.1 mol·L-1的NaHA溶液中c(H+)小于0.1 mol·L-1,加入0.1 mol·L-1KOH溶液至溶液呈中性时消耗的KOH溶液体积小于NaHA溶液体积,则混合溶液中c(Na+)>c(K+);由电荷守恒知,c(Na+)+c(K+)+c(H+)=c(HA-)+2c(A2-)+c(OH-),且c(H+)=c(OH-),则c(Na+)+c(K+)=c(HA-)+2c(A2-);水的离子积与温度有关;混合液中c(Na+)>0.05 mol·L-1;降温、增大c(A2-)都能使平衡CaA(s)??Ca2+(aq)+A2-(aq)左移。废水中加入绿矾和H+,根据流程图,可知发生的是氧化还原反应,配平即可。c(Cr3+)/c(Fe3+)=[c(Cr3+)·c3(OH-)]/[c(Fe3+)·c3(OH)-]=Ksp[Cr(OH)3]/Ksp[Fe(OH)3]=1.5×10-7,故c(Cr3+)=3.0×10-6 mol·L-1。


 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知25℃时部分弱电解质的电离平衡常数数据如下表:
已知25℃时部分弱电解质的电离平衡常数数据如下表:| 化学式 | CH3COOH | H2CO3 | HClO | |
| 平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(H+)?c(CH3COO-) | c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 电解质 | 平衡方程式 | 平衡常数K | Ksp |
| CH3COOH | CH3COOH?CH3COO-+H+ | 1.76×10-5 | |
| H2CO3 | H2CO3?H++HCO3- HCO3-?H++CO32- |
K1=4.31×10-7 K2=5.61×10-11 |
|
| C6H5OH | C6H5OH?C6H5O-+H+ | 1.1×10-10 | |
| H3PO4 | H3PO4?H++H2PO4- H2PO4-?H++HPO42- HPO42-?H++PO43- |
K1=7.52×10-3 K2=6.23×10-8 K3=2.20×10-13 |
|
| NH3?H2O | NH3?H2O?NH4++OH- | 1.76×10-5 | |
| BaSO4 | BaSO4?Ba2++SO42- | 1.07×10-10 | |
| BaCO3 | BaCO3?Ba2++CO32- | 2.58×10-9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com