
【题目】丁苯酞(J)是用于脑血管疾病治疗的药物。它的某种合成路线如下:
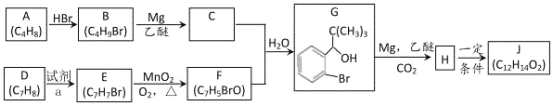
已知: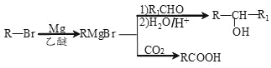
请回答下列问题:
(1)E 的名称为________,F 中所含官能团名称为_______,H→J 的反应类型为_______。
(2)B 生成 A 的方程式_______。
(3)X 是 H 的同系物,相对分子质量比 H 小 56。满足下列条件 X 的同分异构体共有_______种。
①能发生水解反应;②能发生银镜反应;③能与氯化铁溶液发生显色反应。 其中核磁共振氢谱图中有五个吸收峰的同分异构体的结构简式为_______。
(4)利用题中信息所学知识,写出以甲烷和苯甲醛为原料,合成苯乙烯的路线流程图(其他无机试 剂自选)_______。合成路线流程图表达方法例如下:CH2=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH
【答案】邻溴甲苯 或 2-溴甲苯 醛基 溴原子 取代反应 C(CH3)3Br+NaOH![]() CH2=C(CH3)2+NaBr+H2O 13
CH2=C(CH3)2+NaBr+H2O 13 ![]()
![]()
【解析】
D发生取代反应生成E,E发生氧化反应生F,C、F反应生成G,根据G结构简式及F分子式知F为![]() ,逆推得E为
,逆推得E为![]() ,D为
,D为![]() ;根据G结构简式以及F的结构简式再结合题目所给信息可知C为(CH3)3CMgBr,A发生加成反应生成B,B发生信息反应生成C,则A为
;根据G结构简式以及F的结构简式再结合题目所给信息可知C为(CH3)3CMgBr,A发生加成反应生成B,B发生信息反应生成C,则A为![]() ,B为(CH3)3CBr;再根据信息知,H为
,B为(CH3)3CBr;再根据信息知,H为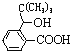 ,根据J分子式知,H发生酯化反应生成J,则J为
,根据J分子式知,H发生酯化反应生成J,则J为 。
。
(1)E为![]() ,E的名称为邻溴甲苯或2-溴甲苯;F为
,E的名称为邻溴甲苯或2-溴甲苯;F为![]() ,F中所含官能团名称为溴原子和醛基;H发生酯化反应或取代反应生成J,则H→J的反应类型为酯化反应或取代反应;
,F中所含官能团名称为溴原子和醛基;H发生酯化反应或取代反应生成J,则H→J的反应类型为酯化反应或取代反应;
(2)A为![]() ,B为(CH3)3CBr,B发生消去反应生成A,反应方程式为C(CH3)3Br+NaOH
,B为(CH3)3CBr,B发生消去反应生成A,反应方程式为C(CH3)3Br+NaOH![]() CH2=C(CH3)2+NaBr+H2O;
CH2=C(CH3)2+NaBr+H2O;
(3)H为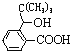 ,X是H的同系物,相对分子质量比H小56,说明比H少4个-CH2,X的同分异构体满足下列条件,①能发生水解反应,说明含有酯基;②能发生银镜反应,说明含有醛基,根据O原子个数知,含有HCOO-;③能与氯化铁溶液发生显色反应,说明含有酚羟基,如果含有HCOO-、-CH3、-OH,有10种结构;
,X是H的同系物,相对分子质量比H小56,说明比H少4个-CH2,X的同分异构体满足下列条件,①能发生水解反应,说明含有酯基;②能发生银镜反应,说明含有醛基,根据O原子个数知,含有HCOO-;③能与氯化铁溶液发生显色反应,说明含有酚羟基,如果含有HCOO-、-CH3、-OH,有10种结构;
如果取代基为HCOOCH2-,-OH,有邻间对3种结构;所以符合条件的有13种;
其中核磁共振氢谱图中有五个吸收峰的同分异构体的结构简式为![]() ;
;
(4)可由![]() 发生消去反应得到苯乙烯,合成
发生消去反应得到苯乙烯,合成![]() 需要苯甲醛与CH3MgBr,甲烷与溴光照得到一溴甲烷,一溴甲烷与Mg、乙醚作用得到CH3MgBr,其合成路线为
需要苯甲醛与CH3MgBr,甲烷与溴光照得到一溴甲烷,一溴甲烷与Mg、乙醚作用得到CH3MgBr,其合成路线为![]() 。
。


科目:高中化学 来源: 题型:
【题目】NO、NO2是大气污染物,但只要合理利用,NO、NO2也是重要的资源。回答下列问题:
(1)氨的合成。已知:N2和H2生成NH3的反应为:![]() N2(g)+
N2(g)+![]() H2(g)
H2(g)![]() NH3(g) ΔH=-46.2kJ·mol-1
NH3(g) ΔH=-46.2kJ·mol-1
在Fe催化剂作用下的反应历程为(※表示吸附态):
化学吸附:N2(g)→2N※;H2(g)![]() 2H※;
2H※;
表面反应:N※+H※![]() NH※;NH※+H※
NH※;NH※+H※![]() NH2※;NH2※+H※
NH2※;NH2※+H※![]() NH3※;
NH3※;
脱附:NH3※![]() NH3(g)
NH3(g)
其中N2的吸附分解反应活化能高、速率慢,决定了合成氨的整体反应速率。则利于提高合成氨平衡产率的条件有(________)
A.低温 B.高温 C.低压 D.高压 E.催化剂
(2)NH3还原法可将NO还原为N2进行脱除。已知:
①4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ΔH1=-1530kJ·mol-1
②N2(g)+O2(g)=2NO(g) ΔH2=+180kJ·mol-1
写出NH3还原NO的热化学方程式__。
(3)亚硝酰氯(ClNO)是合成有机物的中间体。将一定量的NO与Cl2充入一密闭容器中,发生反应:2NO(g)+Cl2(g)![]() 2ClNO(g) △H<0。平衡后,改变外界条件X,测得NO的转化率α(NO)随X的变化如图所示,则条件X可能是__(填字母代号)。
2ClNO(g) △H<0。平衡后,改变外界条件X,测得NO的转化率α(NO)随X的变化如图所示,则条件X可能是__(填字母代号)。
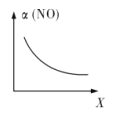
a.温度 b.压强 c.![]() d.与催化剂的接触面积
d.与催化剂的接触面积
(4)在密闭容器中充入4molCO和5molNO发生反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g) △H=-746.5kJmol-1,如图甲为平衡时NO的体积分数与温度、压强的关系曲线图。
N2(g)+2CO2(g) △H=-746.5kJmol-1,如图甲为平衡时NO的体积分数与温度、压强的关系曲线图。
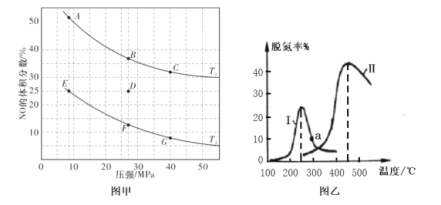
①温度T1__T2(填“>”或“<”)。
②若反应在D点达到平衡,此时对反应进行升温且同时扩大容器体积使平衡压强减小,则重新达到平衡时,D点应向图中A~G点中的__点移动。
③探究催化剂对CO、NO转化的影响。某研究小组将NO和CO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中NO含量,从而确定尾气脱氮率(即NO的转化率),结果如图乙所示。温度低于200℃时,图中曲线I脱氮率随温度升高而变化不大的主要原因为__;a点__(填“
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:①H2(g)+![]() O2(g)=H2O(l) ΔH=-285.8kJ/mol,②H2(g)+
O2(g)=H2O(l) ΔH=-285.8kJ/mol,②H2(g)+![]() O2(g)=H2O(g) ΔH=-241.8kJ/mol,③C(s)+
O2(g)=H2O(g) ΔH=-241.8kJ/mol,③C(s)+![]() O2(g)=CO(g)ΔH=-110.4 kJ/mol,④C(s)+O2(g)=CO2(g) ΔH=-393.5kJ/mol。 回答下列各问:
O2(g)=CO(g)ΔH=-110.4 kJ/mol,④C(s)+O2(g)=CO2(g) ΔH=-393.5kJ/mol。 回答下列各问:
(1)上述反应中属于放热反应的是________。(填序号)
(2)C的燃烧热为_______。
(3)燃烧4g H2生成液态水,放出的热量为______。
(4)写出有关CO燃烧的热化学方程式_______。
(5)比较下面两个热化学方程式中△H的大小: S(s)+O2(g)=SO2(g)△H3,S(g)+O2(g)=SO2(g)△H4 ,△H3 __________△H4
(6)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、____、量筒。量取反应物时,取50 mL 0.50 mol·L-1的盐酸,还需加入的试剂是_______(填序号)。
A 50 mL0.50mol·L-1NaOH溶液 B 50 mL0.55mol·L-1NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质分类是中学化学重要的学科思想。对“一些物质与水反应”的分类图,请按要求填空:
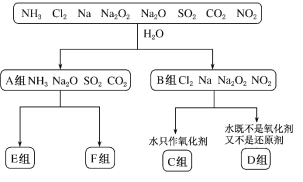
上述分类方法是________________;A组物质中属于电解质的是_____(填化学式);C组物质与水反应的离子方程式为______________________________ ;D组物质与水反应中,氧化剂和还原剂物质的量之比为1∶2的物质是________ (填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
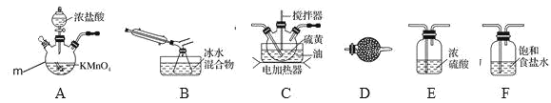
【题目】S2Cl2是一种重要的化工产品。常温时是一种有毒并有恶臭的金黄色液体,熔点-76℃,沸点138℃,受热或遇水分解放热,放出腐蚀性烟气,易与水反应,300℃以上完全分解。进一步氯化可得 SCl2, SCl2 是樱桃红色液体,易挥发,熔点-122℃,沸点 59℃。SCl2与 S2Cl2 相似,有毒并有恶臭,但更不稳 定。实验室可利用硫与少量氯气在 110~140℃反应制得 S2Cl2 粗品。
请回答下列问题:
(1)仪器 m 的名称为______,装置 D 中试剂的作用是______。
(2)装置连接顺序:______→B→D。
(3)为了提高 S2Cl2 的纯度,实验的关键是控制好温度和______。
(4)从 B 中分离得到纯净的 S2Cl2,需要进行的操作是______;
(5)若将S2Cl2放入少量水中会同时产生沉淀和两种气体。某同学设计了如下实验方案,测定所得混合气体中某一成分 X 的体积分数:
![]()
①W 溶液可以是______(填标号)。
a H2O2 溶液 b 氯水 c 酸性 KMnO4 溶液 d FeCl3 溶液
②该混合气体中气体 X 的体积分数为______(用含 V、m 的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25mL0.1mol·L-1某一元碱中,逐滴加入0.1mol·L-1醋酸,滴定曲线如图所示。则下列说法不正确的是
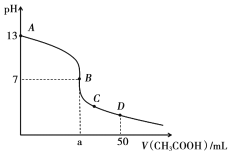
A. 该碱溶液可以溶解Al(OH)3
B. a点对应的体积值大于25mL
C. C点时,c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
D. D点时,c(CH3COO-)+c(OH-)=c(H+)+c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组为研究原电池原理,设计如图甲乙两个原电池装置。

(1)如图甲,a和b用导线连接,Cu电极的电极反应式为:________,溶液中SO42-移向______(填“Cu”或“Fe”)极。
(2)如图乙所示的原电池装置中,负极材料是_____。正极上能够观察到的现象是_______________。 负极的电极反应式是_________________。原电池工作一段时间后,若消耗负极5.4g,则放出气体______mol。
(3)将反应Cu + Fe2(SO4)3=2FeSO4 + CuSO4设计成盐桥电池并画图____________

(4)依据Ba(OH)2·8H2O与NH4Cl晶体的反应原理设计原电池,你认为是否可行并说明理由______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某二元弱酸H2A水溶液中逐滴加入NaOH溶液,混合溶液中lgx(x为![]() 或
或![]() )与pH的变化关系如图所示,下列说法正确的是( )
)与pH的变化关系如图所示,下列说法正确的是( )
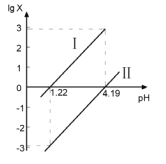
A.pH=7时,存在c(Na+)=c(H2A)+c(HA-)+c(A2-)
B.直线Ⅰ表示的是lg![]() 随pH的变化情况
随pH的变化情况
C.![]() =10-2.97
=10-2.97
D.A2-的水解常数Kh1大于H2A电离常数的Ka2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com